题目内容
实验室常用氯酸钾与二氧化锰混合制取氧气.现将2.5g二氧化锰放入盛有氯酸钾的试管中加热,反应完全结束后,称量固体的质量减少了1.6g.请完成下列问题:
(1)反应结束后,收集到氧气的质量为 g.
(2)计算加热前试管中氯酸钾的质量.
(1) 1.6 g.(2)4.1g
解析试题分析:(1)该反应中,反应物是氯酸钾,生成物是氯化钾和氧气,二氧化锰是催化剂,反应前后质量不变。根据质量守恒定律,化学反应前后物质的总质量不变,氧气是气体会逸散到空气中,所以减少的质量就为氧气的质量,即氧气的质量是1.6g 。
(2)利用化学方程式中氯酸钾与氧气的质量比,结合氧气的质量,可求出氯酸钾的质量
解:设氯酸钾的质量为x
2KClO3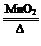 2KCl + 3O2 ↑
2KCl + 3O2 ↑
245 96
X 1.6g
245/96=X/1.6g
解得x=4.1g
答:原氯酸钾的质量的为4.1g。
考点:根据化学反应方程式的计算

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
如图是某试剂瓶标签上的内容.
| 浓硫酸(分析纯) 化学式:H2SO4相对分子质量:98 密度:1.84g∕cm3质量分数;98% |
(1)把这种浓硫酸稀释为溶质质量分数是19.6%的硫酸溶液100g,需要这种硫酸的质量为
(2)将稀释后的硫酸溶液与200g氢氧化钠溶液恰好完全反应,求氢氧化钠溶液的溶质质量分数.