题目内容
(2011?梅州)海水中含氯化钠、氯化镁等物质,是一种重要的自然资源.
(1)从海水中获取淡水,常用的方法是
(2)通过晾晒海水可得到含有较多杂质的氯化钠晶体.氯化钠的用途很广,请写出氯化钠的一种用途
(3)从海水中提取金属镁的流程如下所示:
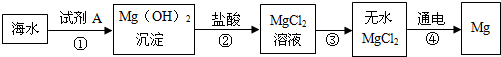
在实际生产中,步骤①加入的试剂A最好选用
(1)从海水中获取淡水,常用的方法是
蒸馏
蒸馏
.(2)通过晾晒海水可得到含有较多杂质的氯化钠晶体.氯化钠的用途很广,请写出氯化钠的一种用途
制纯碱
制纯碱
.(3)从海水中提取金属镁的流程如下所示:

在实际生产中,步骤①加入的试剂A最好选用
Ca(OH)2
Ca(OH)2
(填“NaOH”或“Ca(OH)2”);步骤②中反应的化学方程式为Mg(OH)2+2HCl=MgCl2+2H2O
Mg(OH)2+2HCl=MgCl2+2H2O
.分析:(1)根据物质沸点的差异,一般常用的方法是利用蒸馏来淡化海水;
(2)根据食盐的用途来回答;
(3)氢氧化钙显碱性,能和氯化镁反应生成氢氧化镁沉淀,且氢氧化钙的价格比较经济,而烧碱的碱性强、价格高;根据反应物与生成物来判定发生的化学反应.
(2)根据食盐的用途来回答;
(3)氢氧化钙显碱性,能和氯化镁反应生成氢氧化镁沉淀,且氢氧化钙的价格比较经济,而烧碱的碱性强、价格高;根据反应物与生成物来判定发生的化学反应.
解答:解:(1)因盐类物质的沸点比水高,则从海水中获得淡水,可用的方法是蒸馏,故答案为:蒸馏;
(2)从海水中获得粗盐,可用做工业原料,例如制纯碱,故答案为:制纯碱
(3)氢氧化钙显碱性,能和氯化镁反应生成氢氧化镁沉淀,氢氧化钙的价格比烧碱低,碱性弱,则选择熟石灰,该反应是氢氧化镁与盐酸反应生成氯化镁和水;故答案为:熟石灰;Mg(OH)2+2HCl=MgCl2+2H2O;
(2)从海水中获得粗盐,可用做工业原料,例如制纯碱,故答案为:制纯碱
(3)氢氧化钙显碱性,能和氯化镁反应生成氢氧化镁沉淀,氢氧化钙的价格比烧碱低,碱性弱,则选择熟石灰,该反应是氢氧化镁与盐酸反应生成氯化镁和水;故答案为:熟石灰;Mg(OH)2+2HCl=MgCl2+2H2O;
点评:本题考查从海水中提取镁的流程,学生应注意利用物质的性质并注意利用所选试剂的经济性、碱性等来判断选择试剂的合理性.

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目
