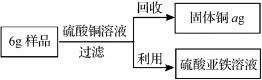
题目内容
【题目】已知常温下NaOH、Na2CO3、NaCl分别在乙醇中的溶解度(S/g)如下表所示:
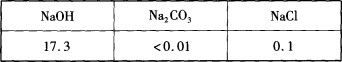
碳酸钠与稀盐酸反应的化学方程式为:Na2CO3+2HCl=2NaCl+CO2↑+H2O
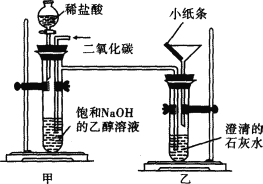
在教师的指导下,小明同学进行了如下图所示的实验。该装置气密性良好,装置乙中的小纸条为湿润的用石蕊溶液染成紫色的纸条。
I.将CO2通人饱和NaOH的乙醇溶液中,直至装置甲的试管中产生沉淀物;
Ⅱ.打开分液漏斗活塞,让稀盐酸缓缓滴人装置甲的试管中;
关于该实验有下列说法:
①饱和NaOH的乙醇溶液中有少量的水
②装置甲的试管中产生的沉淀物为碳酸钠
③装置甲的试管中产生的沉淀物为碳酸钙
④步骤Ⅱ可观察到装置甲的试管中有气泡冒出
⑤实验过程中可观察到装置乙的试管中有沉淀产生
⑥步骤Ⅱ装置乙中的小纸条变蓝色
⑦该实验能验证二氧化碳与氢氧化钠的反应
以上说法正确的是( )
A.①②④⑤ B.①③⑤⑥ C.②④⑤⑦ D.④⑤⑥⑦
【答案】C
【解析】
试题分析:饱和NaOH的乙醇溶液中没有少量的水,因为溶剂是酒精;装置甲的试管中产生的沉淀物为碳酸钠,因为碳酸钠在酒精中的溶解度为0.01克,难溶于酒精;装置甲的试管中产生的沉淀物不可能为碳酸钙,因为过程中没有钙元素;步骤Ⅱ可观察到装置甲的试管中有气泡冒出,因为碳酸钠和盐酸反应会产生二氧化碳气体;实验过程中可观察到装置乙的试管中有沉淀产生,因为二氧化碳会和氢氧化钙发生反应变为碳酸钙沉淀;步骤Ⅱ装置乙中的小纸条变红色,因为二氧化碳会和水发生反应,产生碳酸;该实验能验证二氧化碳与氢氧化钠的反应。故选C.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目