题目内容
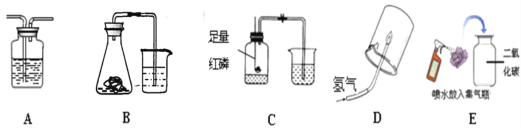
【题目】下图是实验室制取气体的常用装置,请回答下列问题。
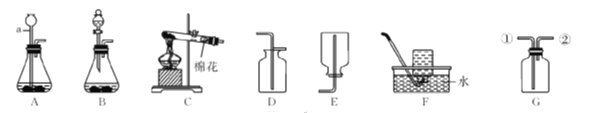
(1)写出图中仪器a的名称:____________。
(2)实验室用加热高锰酸钾制取氧气的化学方程式为________________________________________________,可选择的发生装置为______(填字母)。
(3)用D装置收集二氧化碳时,检验气体是否验满的方法及现象是______________________________________________。
(4)实验室用石灰石和稀盐酸反应制取二氧化碳的化学方程式为________________________________________________________________________,该反应生成的二氧化碳气体中常混有少量氯化氢气体,可通过盛有饱和碳酸氢钠溶液的G装置除去氯化氢气体,则该混合气体应从G装置的______口(填“①”或“②”)通入。
【答案】长颈漏斗2KMnO4![]() K2MnO4+MnO2+O2↑C将燃着的小木条放在集气瓶口,若木条立即熄灭,则已收集满CaCO3+2HCl=CaCl2+H2O+CO2↑①
K2MnO4+MnO2+O2↑C将燃着的小木条放在集气瓶口,若木条立即熄灭,则已收集满CaCO3+2HCl=CaCl2+H2O+CO2↑①
【解析】
(1)据图可以看出,a是长颈漏斗;
(2)用高锰酸钾制取氧气的化学方程式为2KMnO4![]() K2MnO4+MnO2+O2↑,该反应是固体加热型反应,应选择的发生装置是A;
K2MnO4+MnO2+O2↑,该反应是固体加热型反应,应选择的发生装置是A;
(3)用排空气法收集二氧化碳时,检验集气瓶是否收集满的方法是:将燃着的木条放在集气瓶口,木条熄灭,证明集满;
(4)实验室用石灰石和稀盐酸反应制取二氧化碳,化学方程式为 CaCO3+2HCl═CaCl2+H2O+CO2↑,该反应生成的二氧化碳中常混有少量氯化氢气体,可通过盛有饱和碳酸氢钠溶液的G装置除去氯化氢气体,则该混合气体应从G装置的长管通入,即 ①口通入。

【题目】联系所学的![]() 的性质,结合以下短文的相关信息,回答相关问题:
的性质,结合以下短文的相关信息,回答相关问题:
![]() 年,美国科学家卡尔克里斯特领导的研究小组成功地制取出盐粒大小的氮
年,美国科学家卡尔克里斯特领导的研究小组成功地制取出盐粒大小的氮![]() (化学式为
(化学式为![]() ).在制取氮
).在制取氮![]() 的实验中,它曾发生了爆炸,摧毁了实验室的部分设备.因此,科学家们认为,如果能让这种物质保持稳定;则它可能会成为火箭和导弹后级的理想燃料.氮
的实验中,它曾发生了爆炸,摧毁了实验室的部分设备.因此,科学家们认为,如果能让这种物质保持稳定;则它可能会成为火箭和导弹后级的理想燃料.氮![]() 是由排列成
是由排列成![]() 形的
形的![]() 个氮原子结合而成的,化学性质极不稳定.
个氮原子结合而成的,化学性质极不稳定.
![]() 比较氮气和氮
比较氮气和氮![]() 的异同点:
的异同点:
氮气 | 氮 | ||
不同点 | 分子构成 | ________ | ________ |
物理性质 | ________ | ________ | |
化学性质 | ________ | ________ | |
相同点 | _____________________________________ | ||
![]() 请你想象一下
请你想象一下![]() 在应用领域有哪些用途?(至少写
在应用领域有哪些用途?(至少写![]() 条)________,________.
条)________,________.