题目内容
【题目】小茗同学取14%的硫酸溶液70 g于烧杯中,然后向烧杯中慢慢加入10 g氧化铜粉末并不断搅拌,测得烧杯中溶液的质量与加入氧化铜粉末的质量关系如图所示。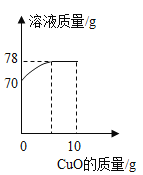
(1)完全反应时共消耗氧化铜的质量是__________。
(2)求反应后所得溶液的溶质质量分数______。
(3)配制14%的硫酸溶液70 g,需要98%的浓硫酸的质量为____________。
【答案】8g20.5%10g
【解析】
(1)氧化铜和硫酸反应生成硫酸铜和水,所以溶液质量增加的就是氧化铜的质量,所以氧化铜的质量=78g-70g=8g;
(2)设当加入49g稀硫酸溶液时恰好完全反应,生成硫酸铜的质量为x,
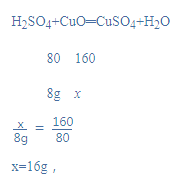
所以溶液中溶质的质量分数=![]() ×100%≈20.5%,
×100%≈20.5%,
(3)设需要98%的硫酸质量为y,则:70g×14%=y×98%,y=10g。

练习册系列答案
相关题目