题目内容
【题目】铜在潮湿的空气中会生锈生成铜绿,铜绿的主要成分为碱式碳酸铜(化学式:Cu2(OH)2CO3),
铜绿的成分有多种,其化学式也可表示为xCu(OH)2·yCuCO3。
(1)孔雀石呈绿色,是一种名贵的宝石,其主要成分是Cu(OH)2·CuCO3。某兴趣小组为探究制取孔雀石的最佳反应条件,设计了如下实验:
(已知:2Cu(NO3)2+2NaOH+Na2CO3===Cu(OH)2·CuCO3↓+4NaNO3
实验1:将2.0mL9.0%的Cu(NO3)2溶液、2.0mlL2.0%的NaOH溶液和2.0%的Na2CO3溶液按表I所示体积混合,实验记录如下
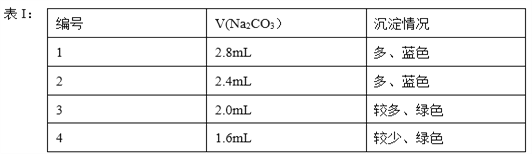
实验2:将合适比例的混合物在表Ⅱ所示温度下反应,实验记录如下。
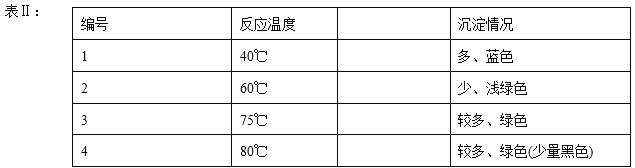
①为了避免铜生锈,铜应尽量保存在______________________;
②实验室制取少许孔雀石,应该采用的最佳温度条件是_______________;
③80℃时,所制得的孔雀石有少量黑色物质的可能原因是_____________。
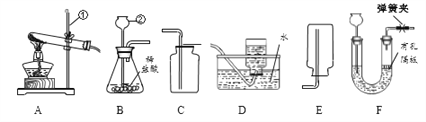
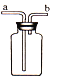
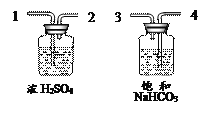
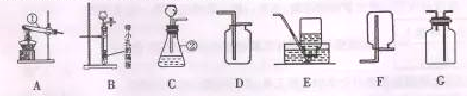
(2)实验小组为测定上述某条件下所制得孔雀石(xCu(OH)2·yCuCO3)样品组成,利用下图所示的装置(夹持仪器省略)进行实验: (已知:碱石灰能吸收二氧化碳和水,浓硫酸有吸水性)
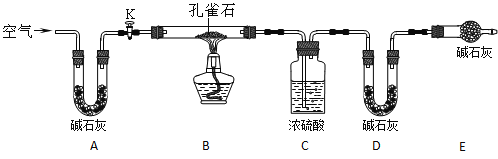
①装置E中碱石灰的作用是____________________;
②充分反应后,某同学在实验过程中采集了如下数据:
a.反应前玻璃管与样品的质量163.8g; b.反应后玻璃管中残留固体质量56.0g;
c.装置C实验后增重9.0g; d.装置D实验后增重8.8g
根据上述有关数据及计算结果,写出该样品组成的化学式______________。
【答案】 在干燥的环境中 75℃ 部分碱式碳酸铜受热分解生成了氧化铜 防止空气中的二氧化碳和水蒸气进入装置D 5Cu(OH)2·2CuCO3
【解析】本题考查了孔雀石制备和样品组成,涉及了根据化学方程式计算分析物质组成,浓硫酸增重的质量是生成的水的质量,碱石灰增重的质量是生成的二氧化碳的质量。
(1)①铜的锈蚀是铜与空气中的氧气,水和二氧化碳的共同作用形成的。为了避免铜生锈,铜应尽量保存在在干燥的环境中;
②根据表Ⅱ75℃时,产生的孔雀石最多,杂质最少。实验室制取少许孔雀石,应该采用的最佳温度条件是75℃;
③80℃时,所制得的孔雀石有少量黑色物质的可能原因是部分碱式碳酸铜受热分解生成了氧化铜;
(2) ①碱石灰能吸收二氧化碳和水。装置E中的作用是防止空气中的二氧化碳和水蒸气进入装置D,影响实验结果。
②孔雀石受热分解的化学方程式是:xCu(OH)2·yCuCO3) ![]() (x+y)CuO+xH2O+yCO2↑
(x+y)CuO+xH2O+yCO2↑
根据化学方程式可知装置C实验后增重的质量中产生的水质量;装置D实验后增重的质量是反应产生的二氧化碳质量。
xCu(OH)2·yCuCO3) ![]() (x+y)CuO+xH2O+yCO2↑
(x+y)CuO+xH2O+yCO2↑
18x 44y
9g 8.8g
![]() x:y=5:2所以样品组成的化学式为5Cu(OH)2·2CuCO3。
x:y=5:2所以样品组成的化学式为5Cu(OH)2·2CuCO3。

 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案【题目】下表提供的四组物质符合图示相连物质间在一定条件下可以发生反应的是
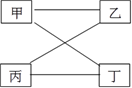
甲 | 乙 | 丙 | 丁 | |
A | CO | O2 | H2SO4 | CuO |
B | Mg | HCl | CuSO4 | NaOH |
C | KOH | SO3 | NaOH | CuSO4 |
D | Na2CO3 | Ca(OH)2 | HCl | CaCl2 |
A. A B. B C. C D. D