题目内容
【题目】同学用下列两个装置进行实验验证“加热碳酸氢铵”后的产物。回答下列问题:
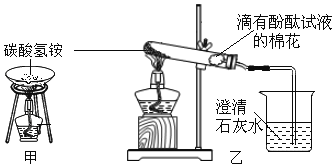
(1)甲实验中发生的化学反应方程式为___________;
(2)乙实验中的实验现象除了固体逐渐消失、试管内壁有少量水珠外,烧杯中的现象是___________,反应的化学反应方程式_____;乙实验结束时,在熄灭酒精灯时最好应先_____;目的是____;
(4)相对于甲实验来说,乙实验的优点有(写一条)__________________。
【答案】 NH4HCO3![]() NH3↑ +CO2 ↑+H2O 澄清石灰水变浑浊 CO2+Ca(OH)2==CaCO3 ↓+H2O 将导管移出,防止倒吸 可检验产物 在密闭容器中不污染空气。
NH3↑ +CO2 ↑+H2O 澄清石灰水变浑浊 CO2+Ca(OH)2==CaCO3 ↓+H2O 将导管移出,防止倒吸 可检验产物 在密闭容器中不污染空气。
【解析】本题主要考查了碳酸氢铵和二氧化碳的性质。
(1)甲实验中发生的化学反应是碳酸氢铵分解生成了氨气、水和二氧化碳,方程式为NH4HCO3![]() NH3↑ +CO2 ↑+H2O;
NH3↑ +CO2 ↑+H2O;
(2)二氧化碳能使澄清石灰变浑浊,烧杯中的现象是澄清石灰变浑浊,反应的化学方程式是CO2+Ca(OH)2==CaCO3 ↓+H2O;乙实验结束时,在熄灭酒精灯时最好应先将导管移出;目的是防止倒吸;
(4)相对于甲实验来说,乙实验的优点有可检验产物、在密闭容器中不污染空气。

【题目】水善利万物
(1)水的组成:
下图是水电解实验,由此获得的信息是:
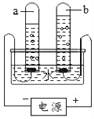
①a、b两极气体体积比为___________;
②该反应的化学方程式是____________。
(2)水的净化:
①生活中常通过____________方法降低水的硬度;
②经家用电解离子水器净化可得到酸、碱性不同的水,且各有其用途:
水的应用 | 浸泡蔬菜 | 日常饮用 | 烹饪 | 洗涤器皿 |
pH | 10.0 | 9.5 | 9.0 | 5.5 |
取上表用于____________的水样品中,滴入石蕊试液变红色。
(3)水的用途:
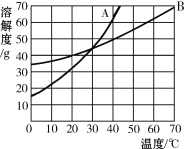
水是常见溶剂,下图为甲、乙、丙三种物质的溶解度曲线;
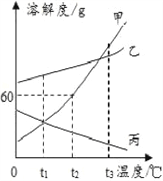
t1℃时,甲、乙、丙三种物质的溶解度大小关系是__________;
②t2℃时,甲的饱和溶液中溶质和溶剂的质量比为____________。