题目内容
【题目】足量的CO还原10.0g工业铁红(主要成分是Fe2O3,还含有少量的FeO、Fe3O4),将生成的气通入足量的Ca(OH)2溶液中,产生50.0g沉淀。则此铁红中铁元素的质量分数是
A. 32% B. 20% C. 76% D. 85%
【答案】B
【解析】设反应生成二氧化碳质量为x,
由Fe2O3+3CO ![]() 2Fe+3CO2,FeO+CO
2Fe+3CO2,FeO+CO ![]() Fe+CO2,Fe3O4+4CO
Fe+CO2,Fe3O4+4CO ![]() 3Fe+4CO2可知,二氧化碳中的氧元素一半来自于铁的氧化物,
3Fe+4CO2可知,二氧化碳中的氧元素一半来自于铁的氧化物,
Ca(OH)2+CO2═CaCO3↓+H2O,
44 100
x 15.0g
![]()
x=22g,
二氧化碳中氧元素质量为:22g×![]() ×100%=16g,
×100%=16g,
铁红中氧元素质量为:16g÷2=8g,
铁元素质量分数为: ![]() ×100%=20%,故选B。
×100%=20%,故选B。

 金钥匙试卷系列答案
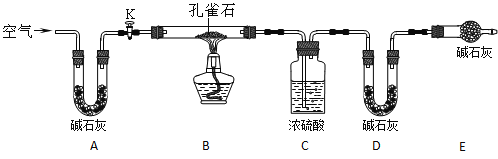
金钥匙试卷系列答案【题目】根据图中实验装置,回答问题:
发生装置 | 收集装置 | 洗气装置 |
|
|
|
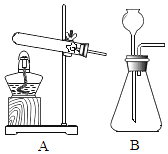
(1)仪器a的名称是________.
(2)用A装置制取氧气的化学方程式为________,收集装置为(填字母序号)________.
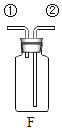
(3)实验室制取二氧化碳的化学反应方程式为________,若用F装置收集二氧化碳,则气体应从F装置的________(填“①”或“②”)端口通入.
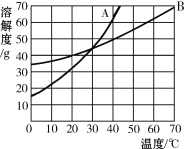
【题目】已知常温下NaOH、Na2CO3、NaCL分别在乙醇中的溶解度(S/g)如下表所示:
在教师的指导下,小明同学进行了如图所示的实验,该装置气密性良好,装置乙中的小纸条为湿润蓝色石蕊试纸。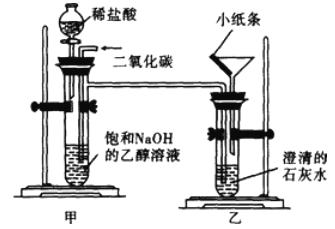
NaOH | Na2CO3 | NaCl |
17.3 | <0.01 | 0.1 |
I.将CO2通入饱和NaOH的乙醇溶液中,装置甲的试管中产生沉淀物;
II.打开分液漏斗活塞,让稀盐酸缓缓滴入装置甲的试管中;
关于该实验有下列说法:
①饱和NaOH的乙醇溶液中溶质是乙醇
②装置甲的试管中产生的沉淀物为碳酸钠
③装置甲的试管中产生的沉淀物为碳酸钙
④步骤II可观察到装置甲的试管中有气泡冒出
⑤实验过程中可观察到装置乙的试管中有沉淀产生
⑥步骤II装置乙中的小纸条变紫色
⑦该实验能验证二氧化碳与氢氧化钠的反应以上说法正确的是
A. ①②④⑤ B. ①③⑤⑥ C. ②④⑤⑦ D. ④⑤⑥⑦
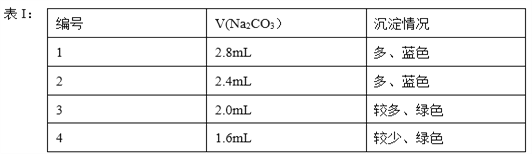
【题目】某研究小组为探究“影响铁制品锈蚀快慢的因素”,取同浓度的稀氨水和稀醋酸,用右图装置完成表中实验,回答下列问题。
![]()
实验序号 | ① | ② | ③ | ④ |
实验温度/℃ | 25 | 25 | 70 | 70 |
试剂 | 稀氨水 | 稀醋酸 | 稀氨水 | 稀醋酸 |
出现铁锈 所需时间 | 1天 未见锈蚀 | 5分钟 | 1天 未见锈蚀 | 1分钟 |
(1)铁锈的主要成分是________(填化学式)。
(2)实验②和④可探究________因素对铁制品锈蚀快慢的影响;欲探究试剂酸碱性对铁制品锈蚀快慢的影响,应选择的实验是______________(填实验序号)。
(3)根据表中实验现象得出的结论是_________________(写出1点即可)。
(4)影响铁制品的锈蚀快慢除上述因素外,还有______________________(写出1点即可),请设计实验方案_________________________________________________。