题目内容
【题目】(题文)如图是某种胃药的部分标识,胃药中所含的物质能中和胃里过多的胃酸(主要 是盐酸)。某患者按标识上的服用方法服药,服药三天后病情好转。计算患者在三天内所服的此胃药中:

(1)所含 Al(OH)3 的质量_____;
(2)理论上可中和胃酸中 HCl 的质量为多少_______?
【答案】 4500mg 6317.3mg
【解析】本题考查了根据化学反应方程式的计算。注意解题的步骤的规范。
(1)服用三天共摄入体内氢氧化铝质量为 3×3×2×250mg=4500mg,
(2)设参加反应HCl质量为x
Al(OH)3+3HCl=AlCl3+3H2O
78 109.5
4500mg x
![]() 解得 x≈6317.3mg
解得 x≈6317.3mg
答:(1)所含Al(OH)3的质量是4500mg;
(2)理论上可中和胃酸中的HCl质量是6317.3mg。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
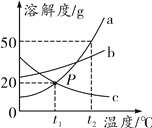
【题目】图表法是一种常用的数据处理方法,根据所给图表(氢氧化钠、碳酸钠分别在水、酒精中的溶解度如表所示),下列说法正确的是( )
氢氧化钠 | 碳酸钠 | |||
20℃ | 40℃ | 20℃ | 40℃ | |
水 | 109g | 129g | 21.8g | 49g |
酒精 | 17.3g | 40g | 不溶 | 不溶 |

A. 上述图象表示碳酸钠的溶解度曲线
B. 20℃时,氢氧化钠的溶解度大于碳酸钠
C. 40℃时,若将 50g NaOH 分别投入到 100g 水和 100g 酒精中,都能形成饱和溶液
D. 40℃时,将适量 CO2 通入饱和的 NaOH 酒精溶液中,观察不到明显的现象