题目内容
【题目】(6分)芬兰发明家马蒂·努尔米亚发明了一种中和处理二氧化碳的新方法,是将二氧化碳从火力发电厂的烟气中分离出来,放入含有长石成分的水溶液里进行中和处理。在反应过程中,长石的成分不仅能吸收二氧化碳,同时还会生成一些有用的副产品,这些副产品可用作生产铝的原材料和玻璃制造业。其主要流程可示意如下:
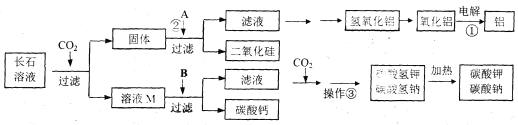
(1)发明家将CO2从火力发电厂的烟气中分离出来,通入含有长石的水溶液里吸收,从环保的角度看,这样做的意义是 ;
(2)长石是地壳中最常见的矿石,含量高达60%。长石主要包括钾长石![]() 、钠长石
、钠长石![]() 、钙长石(
、钙长石(![]() )。若钙长石吸收
)。若钙长石吸收![]() 的反应方程式为:
的反应方程式为:
![]()
请模仿钙长石,写出钠长石吸收CO2的化学反应方程式 ;
(3)若A的pH小于7,试写出一个符合反应②的化学方程式 ;
(4)溶液M中的溶质为 ,B可用作改良酸性土壤,则B为 _ ;操作③主要目的为 。
【答案】(1)减少二氧化碳的排放,减缓温室效应;
(2)NaAlSi3O8+CO2 +2H2O= NaHCO3+3SiO2↓+ Al(OH)3↓;
(3)Al(OH)3+3HCl=AlCl3+3H2O;
(4)Ca(HCO3)2 NaHCO3 KHCO3 ; Ca(OH)2 从溶液中提取晶体
【解析】
试题分析:(1)空气中二氧化碳含量增多会造成温室效应,发明家将CO2从火力发电厂的烟气中分离出来,通入含有长石的水溶液里吸收,可减少二氧化碳的排放,减缓温室效应。
(2)根据钙长石吸收二氧化碳的化学方程式,将其中的钙元素换成钠元素,正确写出对应化学式,然后配平化学方程式即可NaAlSi3O8+CO2+2H2O=NaHCO3+3SiO2↓+Al(OH)3↓。
(3)A的pH值小于7,能和固体氢氧化铝反应,则A可以是酸,符合反应②的化学方程式可以为Al(OH)3+3HCl=AlCl3+3H2O;
(4)长石中含有钾长石(KAlSi3O8)、钠长石(NaAlSi3O8)、钙长石(CaAl2Si2O8)钙长石溶液中通入二氧化碳后生成碳酸氢钾、碳酸氢钠、碳酸氢钙,过滤后得到的溶液M中含有的溶质为KHCO3、NaHCO3、Ca(HCO3) 2,氢氧化钙可用作改良酸性土壤,氢氧化钙与KHCO3、NaHCO3、Ca(HCO3) 2反应生成碳酸钙沉淀,过滤后滤液中含有碳酸钠、碳酸钾,通入二氧化碳后生成碳酸氢钠、碳酸氢钾,要得到碳酸氢钠和碳酸氢钾固体,需蒸发溶剂,从溶液中提取出两种晶体,然后加热后得到碳酸钠、碳酸钾。

 巧学巧练系列答案
巧学巧练系列答案