题目内容
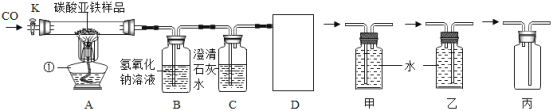
【题目】A、B、C、D、E是初中所学的常见物质。B、C、D常温下为气体,且B、C组成元素相同,A、E是黑色粉末。它们转化关系如下(部分物质及反应条件省略):
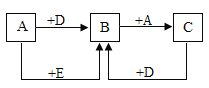
(1)A的化学式为_______________;C的化学式为_____________;
(2)写出A+E反应的化学方程式___________________________________;写出B+A反应的化学方程式___________________;属于__________反应;
(3)列举一例B在生活中的用途__________________。
【答案】C CO C+ 2CuO ![]() 2Cu + CO2↑ C+ CO2
2Cu + CO2↑ C+ CO2 ![]() 2CO 化合 灭火剂等
2CO 化合 灭火剂等
【解析】
B、C、D常温下为气体,且B、C组成元素相同,一氧化碳和二氧化碳都是由碳、氧元素组成的,在常温下都为气体,A、E是黑色粉末,碳在氧气中充分燃烧生成二氧化碳,二氧化碳和碳在高温下反应生成一氧化碳,碳和氧化铜在高温下反应生成铜和二氧化碳,一氧化碳在氧气中燃烧生成二氧化碳,碳和氧化铜都是黑色固体,A是碳,D是氧气,B是二氧化碳,C是一氧化碳,E是氧化铜。
(1)A、E是黑色粉末,碳在氧气中充分燃烧生成二氧化碳,二氧化碳和碳在高温下反应生成一氧化碳,碳和氧化铜在高温下反应生成铜和二氧化碳,一氧化碳在氧气中燃烧生成二氧化碳,碳和氧化铜都是黑色固体,A是碳,故A的化学式为C;C是一氧化碳,C的化学式为CO。
(2)A+E反应是碳和氧化铜高温生成铜和二氧化碳,反应的化学方程式为C+ 2CuO ![]() 2Cu + CO2↑;B+A反应是碳和二氧化碳高温生成一氧化碳,反应的化学方程式为C+ CO2
2Cu + CO2↑;B+A反应是碳和二氧化碳高温生成一氧化碳,反应的化学方程式为C+ CO2 ![]() 2CO;反应符合多变一,故属于化合反应。
2CO;反应符合多变一,故属于化合反应。
(3)B是二氧化碳,B在生活中的用途是灭火剂等。

 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案【题目】某化学兴趣小组为探究金属铝和铜的活动性强弱,开展了以下活动。
(查阅资料)
a.经查阅,金属铝在常温下能与空气中的氧气反应生成致密的氧化铝薄膜。
b.铜、铁、铝都不溶于水;
c.硫酸铜、硫酸亚铁、硫酸铝都溶于水
(对比实验)
编号 | 操作 | 现象 |
甲 | 将表面未打磨的铝丝浸入CuSO4溶液中 | 无明显现象 |
乙 | 将表面打磨后的铝丝浸入CuSO4溶液中 | 铝丝表面析出红色固体 |
丙 | 将表面未打磨的铝丝浸入CuCl2溶液中 | 铝丝表面析出红色固体 |
(1)比较实验乙和实验_________(填“甲”或“丙”)可得知:打磨能破坏氧化铝薄膜。
(2)实验乙中反应的化学方程式为______,据此可知金属活动性Al比Cu____(填强”或“弱”)。
(3)根据所学的知识,小红设计了另一种判断铝和铜活动性强弱的方案,请你帮她填空
实验操作 | 实验现象 | 实验结论 |
将表面打磨过的铝丝和铜丝同时浸入到_____中 | _________ | 与上述实验结论相同 |
(4)在进行乙中实验的过程中,下列图像正确的是________
a. b.
b.
c. d.
d.
(拓展延伸)
小明同学提出一个问题:如果将铝粉和铁粉同时放入到一定量的硫酸铜溶液中,充分反应后所得固体是什么?
小红的猜想:只有铜 小宁的猜想:铜和铁
小童的猜想:铜、铁、铝 小红的猜想:铜和铝
上述猜想肯定错误的是________________的猜想。做出这种判断的依据是,在金属活动性顺序里,位于前面的金属能把位于后面的金属从它们的化合物溶液中置换出来。