题目内容
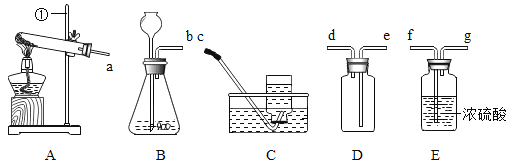
【题目】要配置50g溶质质量分数为15%的氯化钠溶液的实验步骤:
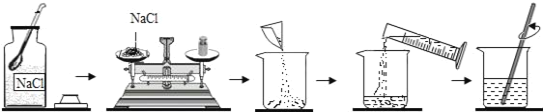
(1)计算:需要氯化钠的质量是_____;需要水的质量是_____;需要水的体积是_____;
(2)称量:称取食盐时,发现指针偏右,应该进行的操作是_____,把称好的食盐倒入烧杯;量取水时,应该选择_____的量筒(填10mL;50mL;100mL),读数时若仰视凹液面的最低处,则量取的水的体积要比需要的_____(填“多”、“少”、“不变”);
(3)把量取的水倒入盛食盐的烧杯中,用玻璃棒搅拌,目的是_____;
(4)把溶解得到的食盐水倒入试剂瓶,放到指定位置.
【答案】7.5g 42.5g 42.5mL 增加食盐 50 mL 多 加速溶解
【解析】
(1)50g 15%的氯化钠溶液中氯化钠的质量=50g×15%=7.5g,该溶液中溶剂水的质量=50g﹣7.5g=42.5g,水的体积是42.5mL;
(2)称取食盐时,发现指针偏右,说明药品少,所以要增加食盐;选取量筒时,要选择比量取的液体体积大,且最接近的,所以量取42.5mL水,需要用50mL量筒;仰视读数偏小,但量取到的实际液体偏大,所以量取的水的体积要比需要的多;
(3)玻璃棒的作用是搅拌,加速食盐溶解。

【题目】在一次聚餐中,同学们对燃料“固体酒精”产生了兴趣,于是对该固体酒精的成分进行探究。
(查阅资料)(1)固体酒精由酒精、氯化钙和氢氧化钠按一定质量比例混制成。
(2)氯化钙溶液呈中性,碳酸钠溶液呈碱性。
(提出问题)(1)酒精中是否含有碳元素?
(2)该固体酒精中的氢氧化钠是否变质?
(实验探究)(1)按如图实验,发现澄清石灰水变浑浊,可得出酒精中含有碳元素的结论,此结论_____(填“合理”或“不合理”)
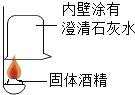
(2)取少量该固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀,取沉淀于试管中加稀盐酸,有气泡产生,该气体是_____。
(实验结论)分析实验并结合资料得出氢氧化钠已变质。
(拓展实验)为进一步确定氢氧化钠的变质程度,小北同学做了以下实验:
实验方案 | 实验现象 | 实验结论 |
取烧杯中上层清液于试管中,加入几滴酚酞溶液 | 溶液变红 | 清液中有氢氧化钠 |
另取烧杯中上层清液于试管中,加入澄清石灰水溶液 | 产生_____ | 清液中有碳酸钠 |
(1)有同学认为小北的实验不能证明清液中一定有氢氧化钠,理由是_____。
(2)该同学另取烧杯中上层清液,加入足量的氯化钙溶液充分反应,有白色沉淀生成,反应后滴加酚酞溶液,溶液变红,加入足量氯化钙溶液的目的是_____,写出生成沉淀的化学方程式:_____。
(3)实验结论:固体酒精中氢氧化钠的变质程度是_____(填“完全变质”或者“部分变质”)
【题目】物质的溶解性受到各种因素的影响,请根据下列信息回答问题:
表一:常温下,一些物质在水中的溶解度
Ba(NO3)2 | BaCl2 | AgCl | AgNO3 | |
水 | 9.2g | 33.3g | 0.00015g | 170.0g |
表二:常温下,一些物质在乙醇中的溶解度
Ba(NO3)2 | BaCl2 | NaOH | NaCl | Ca(NO3)2 | CaCl2 | |
乙醇 | 0.002g | 4.1g | 14.7g | 0.07g | 33.9g | 20.5g |
(1)表一、表二数据说明物质的溶解性受到_____等因素的影响。
(2)常温下,40g水中加入2gBa(NO3)2固体,充分溶解,得到溶液质量为_____g。
(3)酸、碱、盐在溶液中发生复分解反应的条件是有沉淀析出、或有气体放出、或有水生成。请回答
①表一中物质在水中发生复分解反应的化学方程式_____。
②表二中物质在乙醇中发生复分解反应的化学方程式_____。从微观的角度看,溶液中减少的微粒是_____(写微粒符号)。