题目内容
【题目】某学习小组对旧铜器上的绿色锈斑产生了探究兴趣。
(一)对绿色锈斑的探究
(查阅资料)①无水硫酸铜为白色粉末,遇水变蓝;②碱石灰是 CaO 和 NaOH 的固体混合物;③绿色锈斑 的主要成分是碱式碳酸铜(Cu2(OH)2CO3),受热易分解。
(探究过程)
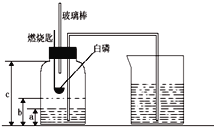
实验1:取一定量的碱式碳酸铜放入试管中并加热,发现试管中的固体由绿色变成黑色,同时试管壁上有无色 液滴出现。
猜想: (1)从元素守恒角度分析,该黑色固体可能是①碳粉;②氧化铜;③ ___________________。
(2)从元素守恒角度分析,生成的气态物质可能是水和 CO2 的混合气体。
实验 2:取少量实验 1 中的黑色固体物质于试管内,加入足量稀硫酸并加热,观察到 ___________________ , 则猜想②正确。
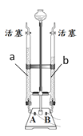
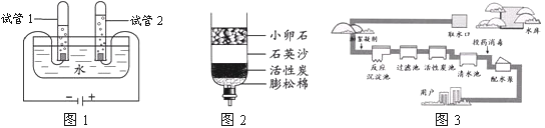
实验 3:同学们选择如下装置探究反应生成的气体成分。

实验步骤:(1)打开 A 中活塞,通入一段时间的空气;
(2)关闭活塞,连接装置,其连接顺序为 A→_____→______________;
(3)点燃酒精灯,充分加热后,停止加热。
现象与结论:根据实验现象可知,碱式碳酸铜分解还生成了二氧化碳和水。
则 A 中玻璃管内反应的化学方程式为 ________________________________________ ;
B 中反应的化学方程式为 _______________________________________________________ ;
反思与评价:A 装置中 U 形管内碱石灰的作用是 _______________________________________ ;
(二)用锈蚀严重的废铜屑为原料,回收铜
资料 1:Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑
资料 2:回收铜的两种实验方案。

反思与评价:
(1)步骤Ⅱ反应的化学方程式为 ____________________________________ 。
(2)溶液 A 中的主要离子有 ____________________________________(写出离子符号)。
(3)理论上两种方案获得铜的质量比较:方案一 ___________________________方案二(选填“>、=、<”)。
(4)方案二优于方案一的理由是_____________________________________________________________(答一点)。
【答案】碳粉和氧化铜的混合物 黑色固体全部溶解形成蓝色溶液 C B Cu2(OH)2CO3 ![]() 2CuO+H2O+CO2↑ CO2+Ca(OH)2=CaCO3↓+H2O 除去空气中的水分和二氧化碳,防止对产物的检验造成干扰 CuO+CO
2CuO+H2O+CO2↑ CO2+Ca(OH)2=CaCO3↓+H2O 除去空气中的水分和二氧化碳,防止对产物的检验造成干扰 CuO+CO![]() Cu+CO2 H+、SO42﹣、Cu2+ = 对环境污染小、节约能源等
Cu+CO2 H+、SO42﹣、Cu2+ = 对环境污染小、节约能源等
【解析】
本题主要考查物质的性质,综合性较强,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论。
(一):探究过程:
(1)从元素守恒角度分析,该黑色固体可能是①碳粉;②氧化铜;③碳粉和氧化铜的混合物;
(2)若猜想②正确,黑色固体中只有氧化铜,没有碳,氧化铜与硫酸在加热时生成了可溶解的氯化铜和水。取少量实验1中的黑色固体物质于试管内,加入足量稀硫酸并加热,观察到黑色固体全部溶解形成蓝色溶液,则猜想②正确;
实验步骤:
(2)根据质量守恒定律,反应生成气体可能有水和二氧化碳,关闭活塞,连接装置时,应该先检验水,后检验二氧化碳,因此其连接顺序为A→C→B;
(3)根据实验现象可知,碱式碳酸铜分解还生成了二氧化碳和水,则A中玻璃管内碱式碳酸铜分解生成了氧化铜、水和二氧化碳,反应的化学方程式为:Cu2(OH)2CO3![]() 2CuO+H2O+CO2↑;B中的反应是二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;
2CuO+H2O+CO2↑;B中的反应是二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;
反思与评价:
本实验是检验碱式碳酸铜分解产物,空气中的水和二氧化碳对实验有干扰。碱石灰能够吸收水蒸气和二氧化碳,因此A装置中U形管内碱石灰的作用是除去空气中的水分和二氧化碳,防止对产物的检验造成干扰;
(二)反思与评价:
(1)步骤Ⅱ中氧化铜和一氧化碳在加热条件下反应生成铜和二氧化碳,反应的化学方程式为:CuO+CO![]() Cu+CO2;
Cu+CO2;
(2)废铜屑中的碱式碳酸铜与硫酸发生了:Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑,溶液A中存在生成硫酸铜和过量的硫酸,溶液A中存在的主要离子有氢离子、硫酸根离子和铜离子,符号分别是:H+、SO42﹣、Cu2+;
(3)理论上两种方案获得铜的质量比较:根据化学反应和质量守恒定律可知,由于都没有铜元素的损失,因此生成的铜的质量是方案一=方案二;
(4)方案二的化学反应是在常温下进行,方案一的化学反应是在加热和高温下进行。方案二优于方案一的理由是对环境污染小、节约能源等。