题目内容
【题目】除去下列各组物质中的杂质,所用试剂和方法均正确的是( )
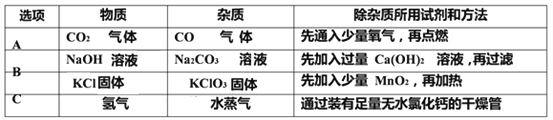
A. A B. B C. C D. D
【答案】D
【解析】
A、除去二氧化碳中的一氧化碳不能够通入氧气点燃,这是因为除去气体中的气体杂质不能使用气体(气体的量不易控制),否则会引入新的气体杂质,错误;B、Na2CO3溶液能与过量Ca(OH)2溶液反应生成碳酸钙沉淀和氢氧化钠,能除去杂质但引入了新的杂质氢氧化钙(过量的),不符合除杂原则,错误;C、KClO3在二氧化锰的催化作用下生成氯化钾和氧气,二氧化锰作催化剂,反应前后质量不变,能除去杂质但引入了新的杂质二氧化锰,不符合除杂原则,错误;D、无水氯化钙具有吸水性,且不与氢气反应,能除去杂质且没有引入新的杂质,符合除杂原则,正确。故选D。

练习册系列答案
相关题目
【题目】请从A或B两题中任选一个作答,若两题均作答,按A计分。
A | B |
|
|
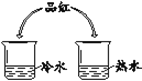
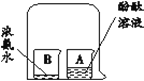
从微粒角度解释: (1)品红在水中扩散的原因是______。 (2)品红在热水中扩散速度快,其原因是______。 | (1)实验现象是______。 (2)实验结论是______。 |