题目内容
味精是烹制菜肴时常用的调味品,其主要成分是谷氨酸钠.谷氨酸钠有鲜味,易溶于水.小明发现某品牌味精包装上标注:“谷氨酸钠含量≥80%,NaCl含量≤20%”.他想测定此味精中NaCl的含量.
查资料:NaCl+AgNO3=AgCl↓+NaNO3,谷氨酸钠的存在不影响NaCl的性质.
实验过程:
①称取该味精样品10.0g,并溶于蒸馏水;
②加入过量的硝酸银溶液;
③过滤;
④用蒸馏水反复洗涤沉淀多次;
⑤将沉淀烘干、称量,测得固体质量为4.3g.
根据上述实验步骤回答下列有关问题:
(1)步骤②中如何检验硝酸银溶液是否过量:________.
(2)过滤操作所需要的仪器除烧杯、铁架台(带铁圈)、玻璃棒外,还需要的玻璃仪器是________.
(3)步骤④中如何检验沉淀是否已洗干净________.
(4)此样品中NaCl的质量分数为________(精确到0.1%),
是否符合其包装上标注的标准?________.
(5)最近专家否认了“味精致癌”的说法,实验表明,味精在100℃时加热半小时,只有0.3%的味精(谷氨酸钠)生成焦谷氨酸钠(有毒),其对人体的影响甚微.对此下列认识正确的是________.
A.谷氨酸钠受热不发生化学变化
B.谷氨酸钠在加热下生成焦谷氨酸钠是物理变化
C.大量食用味精不利于身体健康
D.研究问题的一种有效方法是通过实验.
解:(1)因为氯化钠和硝酸银反应生成氯化银沉淀和硝酸钠,所以如果溶液中仍然有氯化钠,加入硝酸银溶液就会出现沉淀,反之,说明溶液中没有氯化钠,也可以说溶液中硝酸银过量.故答案为:取沉淀后的上层清液少许于试管中,向其中滴加硝酸银溶液,如没有白色不溶物产生即说明硝酸银溶液适量或过量.
(2)根据过滤的仪器可知,过滤一般需要漏斗、玻璃棒、烧杯等,故答案为:漏斗.
(3)因为硝酸银过量,所以沉淀表面有残留的硝酸银.如果洗涤干净啦,则洗涤的液体中就没有硝酸银,因此加入氯化钠就没有沉淀.
(4)根据题目信息可知,沉淀的质量是4.3克,设氯化钠的质量为X.
NaCl+AgNO3=AgCl↓+NaNO3
58.5 143.5
X 4.3g
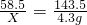
得:X=1.75g
∴样品中NaCl的质量分数=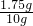 ×100%═17.5%.
×100%═17.5%.
∵17.5%<20%;∴符合包装上的标准.
故答案为:17.5%,符合.
(5)谷氨酸钠在加热下生成焦谷氨酸钠,属于化学变化,故A错误;谷氨酸钠在加热下生成焦谷氨酸钠是化学变化,故B错误;大量食用味精不利于身体健康,故C正确;研究问题的一种有效方法是通过实验,故D正确.故选CD.
故答案为:
(1)取沉淀后的上层清液少许于试管中,向其中滴加硝酸银溶液,如没有白色不溶物产生即说明硝酸银溶液适量或过量.
(2)漏斗; (3)取最后一次洗涤液少许于试管中,向其中滴加氯化钠溶液,如无白色不溶物产生,即说明沉淀已洗干净.
(4)17.5%; 符合;
(5)C、D.
分析:(1)根据氯化钠和硝酸银反应生成氯化银沉淀和硝酸钠即可.
(2)根据过滤的实验仪器即可.
(3)根据氯化钠和硝酸银反应生成氯化银沉淀和硝酸钠即可.
(4)把沉淀质量代入化学方程式计算出氯化钠的质量.
(5)根据所给的信息进行判断作出正确的判断.
点评:鉴定物质的方法一般要求是操作简单,现象明显;掌握过滤的操作方法和所用仪器.
(2)根据过滤的仪器可知,过滤一般需要漏斗、玻璃棒、烧杯等,故答案为:漏斗.
(3)因为硝酸银过量,所以沉淀表面有残留的硝酸银.如果洗涤干净啦,则洗涤的液体中就没有硝酸银,因此加入氯化钠就没有沉淀.
(4)根据题目信息可知,沉淀的质量是4.3克,设氯化钠的质量为X.
NaCl+AgNO3=AgCl↓+NaNO3
58.5 143.5
X 4.3g
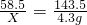
得:X=1.75g
∴样品中NaCl的质量分数=
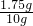 ×100%═17.5%.
×100%═17.5%.∵17.5%<20%;∴符合包装上的标准.
故答案为:17.5%,符合.
(5)谷氨酸钠在加热下生成焦谷氨酸钠,属于化学变化,故A错误;谷氨酸钠在加热下生成焦谷氨酸钠是化学变化,故B错误;大量食用味精不利于身体健康,故C正确;研究问题的一种有效方法是通过实验,故D正确.故选CD.
故答案为:
(1)取沉淀后的上层清液少许于试管中,向其中滴加硝酸银溶液,如没有白色不溶物产生即说明硝酸银溶液适量或过量.
(2)漏斗; (3)取最后一次洗涤液少许于试管中,向其中滴加氯化钠溶液,如无白色不溶物产生,即说明沉淀已洗干净.
(4)17.5%; 符合;
(5)C、D.
分析:(1)根据氯化钠和硝酸银反应生成氯化银沉淀和硝酸钠即可.
(2)根据过滤的实验仪器即可.
(3)根据氯化钠和硝酸银反应生成氯化银沉淀和硝酸钠即可.
(4)把沉淀质量代入化学方程式计算出氯化钠的质量.
(5)根据所给的信息进行判断作出正确的判断.
点评:鉴定物质的方法一般要求是操作简单,现象明显;掌握过滤的操作方法和所用仪器.

练习册系列答案
相关题目
味精是烹制菜肴时常用的调味品,小明发现某品牌味精包装上的部分文字说明.他想测定此味精中氯化钠的含量.(相对原子质量:Na-23 Cl-35.5 Ag-108)
| ××牌味精 主要成分:谷氨酸钠 特性:有鲜味,易溶于水 含量:谷氨酸钠≥80% 氯化钠≤20%查阅资料: NaCl+AgNO3=AgCl↓+NaNO3,谷氨酸钠的存在不影响NaCl的性质. 实验过程: ①称取该味精样品10.0g,并溶于蒸馏水;②加入过量的硝酸银溶液;③过滤;④用蒸馏水反复洗涤沉淀多次;⑤将沉淀烘干、称量,测得固体质量为5.74g.试通过计算确定此样品中NaCl的质量分数与其包装上的标注的含量是否相符. |
 味精是烹制菜肴时常用的调味品,其主要成份是谷氨酸钠.谷氨酸钠有鲜味,易溶于水.小明发现某品牌味精包装上部分标注如右图所示.
味精是烹制菜肴时常用的调味品,其主要成份是谷氨酸钠.谷氨酸钠有鲜味,易溶于水.小明发现某品牌味精包装上部分标注如右图所示. 享受生活离不开化学知识,家庭厨房就是一个充盈的化学小世界,“柴米油盐酱醋糖”中包含着许多化学内容.
享受生活离不开化学知识,家庭厨房就是一个充盈的化学小世界,“柴米油盐酱醋糖”中包含着许多化学内容. (2006?建邺区一模)家庭厨房就是一个充盈的化学小世界,“柴米油盐酱醋糖”中包含着许多化学内容.
(2006?建邺区一模)家庭厨房就是一个充盈的化学小世界,“柴米油盐酱醋糖”中包含着许多化学内容.