题目内容
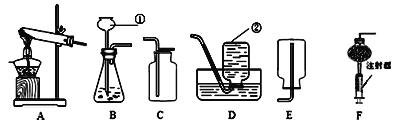
【题目】用金属铁通过一系列转化,可以制备新型消毒、净水剂K2FeO4 . 流程如下:
请回答下列问题:
(1)固体B的成分是(用化学式表示);反应①后经过操作可分别得到固体B和溶液A.
(2)反应①、②、③中没有涉及到的化学基本反应类型是 .
(3)请写出反应②的化学方程式 .
(4)如果所得净水剂K2FeO4的质量为19.8kg,则理论上参加反应的铁的质量为 kg.
【答案】
(1)Cu、Fe ,过滤
(2)分解反应
(3)FeSO4+2KOH= Fe(OH)2↓+K2SO4
(4)5.6
【解析】(1)由反应流程可知,过量铁粉与硫酸铜溶液反应,生成硫酸亚铁和铜,由于铁是过量的,在过滤后得到的固体B是Cu、Fe的混合物; 反应①后得到 固体B和溶液A。故进行的操作是过滤;(2)由反应流程可知,反应①是Fe+CuSO4=Cu+FeSO4,属于置换反应;反应②是FeSO4+2KOH=Fe(OH)2↓+K2SO4,属于复分解反应;反应③是2Fe(OH)2+H2O2= 2Fe(OH)3,属于化合反应。故反应①、②、③中没有涉及到的化学基本反应类型是:分解反应;(3)反应②的化学方程式:FeSO4+2KOH= Fe(OH)2↓+K2SO4;(4)根据分析可知,K2FeO4中铁元素的质量来自参加反应的铁的质量。设参加反应的铁的质量为x。
Fe ~ | K2FeO4 |
56 | 198 |
x | 19.8g |
![]()
x=5.6kg。
所以答案是:Cu、Fe ;过滤;分解反应;FeSO4+2KOH= Fe(OH)2↓+K2SO4;5.6。

 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案【题目】元素X、Y、Z、M是初中化学常见的四种元素。有关信息如表:
元素 | 有关信息 |
X | 可形成相对分子质量最小的气体单质 |
Y | 形成的一种单质是天然存在的最硬的物质 |
Z | 其单质约占空气体积的 |
M | 人体内含量最高的金属元素 |
(1)M元素的名称是_______。
(2)Y形成的天然存在的最硬的物质是_______,此物质不属于________(填“有机物”或“无机物”)。
(3)由X、Y两元素组成的最简单的有机物是______(填化学式),该有机物中X元素的质量分数为______。
(4)由Y、Z两元素组成的能用于人工降雨的固体物质是_______。
(5)由Z、M两元素按原子个数比1∶1组成的化合物,俗称________,写出它与水反应的化学方程式__________ 。