题目内容
【题目】下列四个图象分别与选项中的操作相对应,其中合理的是( )
A. 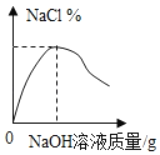 向一定量盐酸中滴加氢氧化钠溶液
向一定量盐酸中滴加氢氧化钠溶液
B. 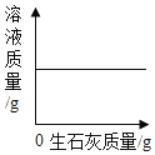 保持温度不变,向一定量的饱和石灰水中加入生石灰
保持温度不变,向一定量的饱和石灰水中加入生石灰
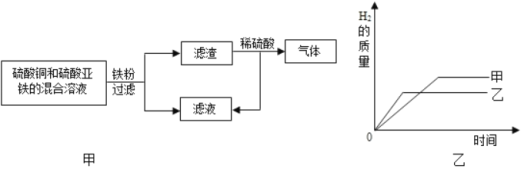
C. 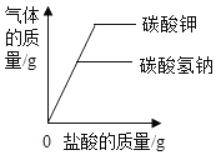 向等质量的碳酸镁和碳酸氢钠中分别加入足量稀盐酸
向等质量的碳酸镁和碳酸氢钠中分别加入足量稀盐酸
D. 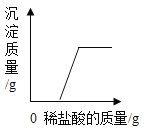 向一定量的有硝酸酸化的硝酸银的混合溶液中滴加稀盐酸
向一定量的有硝酸酸化的硝酸银的混合溶液中滴加稀盐酸
【答案】A
【解析】
A、氢氧化钠和盐酸反应生成氯化钠和水,所以随着氢氧化钠的加入,氯化钠的质量逐渐增大,氯化钠的质量分数也逐渐增大,氢氧化钠和盐酸恰好完全反应,氯化钠的质量分数达到最大值,然后继续氢氧化钠的加入,溶液的质量增大,氯化钠的质量分数会逐渐减小,故A正确;
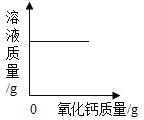
B、氧化钙和水反应生成氢氧化钙,所以向一定量的饱和石灰水中加入生石灰,氧化钙与水反应,溶剂减少,溶质也相应的减少,溶液质量会减小,然后不变,故B错误;
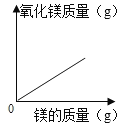
C、碳酸氢钠和碳酸镁中分别加入足量稀盐酸反应的化学方程式分别为:NaHCO3+HCl==NaCl+H2O+CO2↑;MgCO3+2HCl==MgCl2+H2O+CO2↑,碳酸镁和碳酸氢钠的相对分子质量都是84,所以向等质量的碳酸镁和碳酸氢钠中分别加入足量稀盐酸,生成二氧化碳气体的质量相等,故C错误;
D、氯离子和银离子一接触就会生成氯化银沉淀,所以沉淀质量应该从零开始,故D错误。故选A。

【题目】在研究酸和碱的化学性质时,某小组想证明稀硫酸与氢氧化钠溶液混合后,虽然无明显现象,但确实发生了化学反应,试与他们一起完成下列实验。
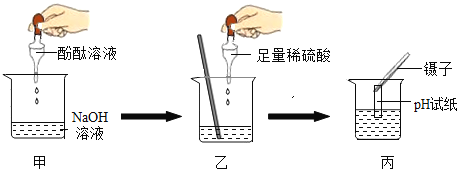
(1)探究稀硫酸与氢氧化钠溶液的反应:
①图甲到图乙的反应现象是_____。
②图中操作存在的问题是_____;若用正确操作测得丙中溶液的pH=5,溶液中溶质的化学式为_____。
(2)探究上述稀硫酸与氢氧化钠溶液反应后烧杯中的硫酸是否过量:
实验方案 | 实验步骤 | 实验现象 | 实验结论 |
方案一 | 取样,滴入适量的氯化钡溶液 | 出现白色沉淀 | 稀硫酸过量 |
方案二 | 取样,滴入几滴紫色石蕊试液 | 溶液变红 | 稀硫酸过量 |
上述设计的实验方案中,正确的是_____,另外一个实验方案错误的原因是_____;请你另选不同种类物质,设计一个确定稀硫酸过量的实验方案_____。
(3)探究氢氧化钠溶液的成分:
某小组同学在进行乙实验时,发现有气泡冒出,他们猜测氢氧化钠溶液可能已经_____(用方程式表示)。于是他们又取了部分反应前的氢氧化钠溶液,加入少量的_____(碱溶液),通过_____现象,确定了自己的猜测。
小组同学对该氢氧化钠溶液的成分产生了兴趣。他们准备对这瓶溶液继续探究。
(作出猜想)小组同学对该氢氧化钠溶液的成分做出了猜想:
猜想1.溶液部分变质 猜想2:_____。
(设计方案)
实验操作 | 实验现象 | 实验结论 | |
方案 | 取少量溶液于试管中,滴加少量澄清石灰水 | 产生白色沉淀 | 猜想1正确 |
取上层清液放入另一只试管中,滴加酚酞溶液 | 溶液变为红色 |
同学们经过讨论,认为该方案不合理,理由是_____:同学们把方案中的某溶液换成了_____溶液,通过实验现象确定了实验结论。