题目内容
【题目】某兴趣小组的同学为测定某石灰石中碳酸钙(假设:石灰石中的杂质不与盐酸反应)的质量分数,称取一定质量的石灰石置于烧杯中,用某浓度的稀盐酸100g,分5次加入,每次充分反应后,取出固体,经过滤、洗涤、干燥等操作后称重,各次稀盐酸用量和剩余固体质量记录如下:
实验次数 | 稀盐酸的用量(g) | 剩余固体的质量(g) |
① | 20 | 16.25 |
② | 40 | 12.50 |
③ | 60 | m |
④ | 80 | 5.00 |
⑤ | 100 | n |
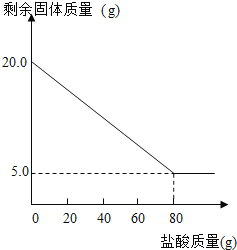
请细心观察表格和图像,回答下列问题:
(1)第_____次石灰石中的碳酸钙与盐酸恰好反应完毕。
(2)表格中m=_____g,n=_____g。
(3)计算该石灰石样品中碳酸钙的质量分数_____。
(4)计算该石灰石样品完全反应生成二氧化碳的质量_____。
【答案】④ 8.75 5.00 75% 6.6g
【解析】
(1)从①②次的数据分析可知,每次剩余固体减少的质量都是3.75g。即每反应盐酸的质量是20g时,消耗的碳酸钙质量是3.75g。所以m=12.5g-3.75g=8.75g,按照此反应情况,④中的固体是恰好完全反应,碳酸钙和稀盐酸反应生成氯化钙和水和二氧化碳。故答案为:④;
(2)因为从①②的反应数据可知,每次剩余固体减少的质量都是3.75g,所以m=12.5g-3.75g=8.75g,根据第四次恰好完全反应可知n=5.00g。故答案为:8.75、5.00;
(3)由图示可知,反应前石灰石的质量是20g,充分反应后,剩余固体物质的质量为5g。所以碳酸钙的质量分数为:![]() 。故答案为:75%;
。故答案为:75%;
(4)因为最后在20g固体中,剩余5g固体是不反应的,所以碳酸钙的质量为:20g-5g=15g。设生成二氧化碳的质量为x。
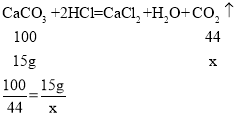
解得x=6.6g。
故答案为:6.6g。

【题目】据统计,我国仅20世纪90年代就发生火灾约89万起,给人民造成重大损失。应用化学知识能有效预防和控制火灾。下面对图中灭火实例的灭火原理解释不正确的是( )

灭火实例 | 灭火原理 | |
A | 住宅失火时,消防队员用水灭火 | 降低可燃物的着火点 |
B | 酒精在桌上着火时,用湿抹布盖灭 | 隔绝空气或氧气 |
C | 炒菜油锅着火时,用锅盖盖熄 | 隔绝空气或氧气 |
D | 扑灭森林火灾时,设置隔离带 | 可燃物与燃烧物隔离 |
A. A B. B C. C D. D
【题目】“分解过氧化氢制氧气的反应中二氧化锰的催化作用”,以及“寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣。
(提出问题)氧化铁能否作过氧化氢溶液分解的催化剂?如果能,其催化效果如何?
(实验探究一)
实验步骤 | 实验现象 |
Ⅰ.分别量取5mL15%过氧化氢溶液放入A、B两支试管中,向A试管中加入ag氧化铁粉末,并分别在A、B两支试管中插入带火星木条,观察现象 | A试管中产生气泡,带火星木条复燃,B试管中无明显现象 |
Ⅱ.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次实验,观察现象。 | 试管中均产生气泡,带火星木条均复燃 |
Ⅲ.将实验Ⅱ中的剩余物小心过滤,并将所得虑渣进行洗涤、干燥、称量,所得固体质量仍为ag | |
Ⅳ.分别量取5mL15%过氧化氢溶液放入C、D两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象 |
(实验原理)请写出实验室用过氧化氢溶液制取氧气的符号表达式_____________;
(实验结论)实验_____、_____分别证明氧化铁的化学性质和质量在反应前后均没有发生变化,可以作过氧化氢分解的催化剂;
(实验评价)
(1)实验设计Ⅳ的目的是___________;
(2)若实验Ⅳ观察到D试管中产生气泡的速率更快,由此你可以得到的结论是__________。
(实验拓展)
(1)通过实验探究对比分析之后,某同学又重新对二氧化锰催化过氧化氢的实验做一探究,所的实验数据如下表所示:
实验次序 | 1 | 2 | 3 | 4 | 5 | 6 |
10%H2O2溶液用量(ml) | 30 | 30 | 30 | 30 | 30 | 30 |
MnO2粉末用量(g) | 0.1 | 0.3 | 0.5 | 0.7 | 0.9 | 1.1 |
完全反应所用时间(s) | 17 | 7 | 4 | 2 | 2 | 2 |
收集到的氧气体积(ml) | 980 | 980 | 980 | 980 | 980 | 980 |
请根据实验数据从不同角度,写出两条结论。_________ 、_________
(2)查阅资料得知,CuO、CuSO4、猪肝、马铃薯等也可以作过氧化氢溶液分解的催化剂。下列有关催化剂的说法中正确的是_________(填字母)。
A MnO2只能作过氧化氢溶液分解的催化剂 B 同一个化学反应可以有多种催化剂
C 催化剂只能加快化学反应的速率 D 用作催化剂的物质不可能是其他反应的反应物或生成物
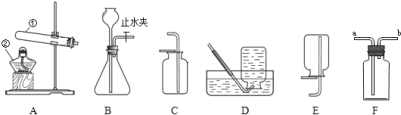
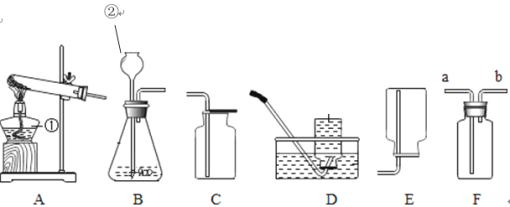
(3)实验室常用氯化铵固体与碱石灰固体共热来制取氨气(NH3)。常温下氨气(NH3)是一种无色、有刺激性气味的气体,密度比空气小,氨气(NH3)极易溶于水。制取并收集氨气(NH3),应该从图中选择的发生装置是______,收集装置是______。