题目内容
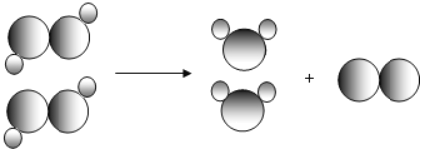
【题目】“分解过氧化氢制氧气的反应中二氧化锰的催化作用”,以及“寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣。
(提出问题)氧化铁能否作过氧化氢溶液分解的催化剂?如果能,其催化效果如何?
(实验探究一)
实验步骤 | 实验现象 |
Ⅰ.分别量取5mL15%过氧化氢溶液放入A、B两支试管中,向A试管中加入ag氧化铁粉末,并分别在A、B两支试管中插入带火星木条,观察现象 | A试管中产生气泡,带火星木条复燃,B试管中无明显现象 |
Ⅱ.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次实验,观察现象。 | 试管中均产生气泡,带火星木条均复燃 |
Ⅲ.将实验Ⅱ中的剩余物小心过滤,并将所得虑渣进行洗涤、干燥、称量,所得固体质量仍为ag | |
Ⅳ.分别量取5mL15%过氧化氢溶液放入C、D两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象 |
(实验原理)请写出实验室用过氧化氢溶液制取氧气的符号表达式_____________;
(实验结论)实验_____、_____分别证明氧化铁的化学性质和质量在反应前后均没有发生变化,可以作过氧化氢分解的催化剂;
(实验评价)
(1)实验设计Ⅳ的目的是___________;
(2)若实验Ⅳ观察到D试管中产生气泡的速率更快,由此你可以得到的结论是__________。
(实验拓展)
(1)通过实验探究对比分析之后,某同学又重新对二氧化锰催化过氧化氢的实验做一探究,所的实验数据如下表所示:
实验次序 | 1 | 2 | 3 | 4 | 5 | 6 |
10%H2O2溶液用量(ml) | 30 | 30 | 30 | 30 | 30 | 30 |
MnO2粉末用量(g) | 0.1 | 0.3 | 0.5 | 0.7 | 0.9 | 1.1 |
完全反应所用时间(s) | 17 | 7 | 4 | 2 | 2 | 2 |
收集到的氧气体积(ml) | 980 | 980 | 980 | 980 | 980 | 980 |
请根据实验数据从不同角度,写出两条结论。_________ 、_________
(2)查阅资料得知,CuO、CuSO4、猪肝、马铃薯等也可以作过氧化氢溶液分解的催化剂。下列有关催化剂的说法中正确的是_________(填字母)。
A MnO2只能作过氧化氢溶液分解的催化剂 B 同一个化学反应可以有多种催化剂
C 催化剂只能加快化学反应的速率 D 用作催化剂的物质不可能是其他反应的反应物或生成物
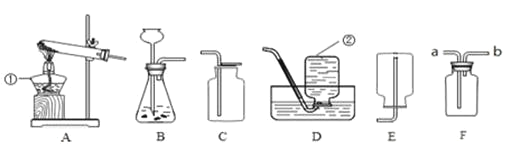
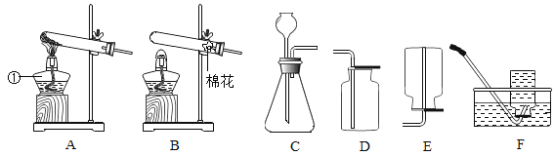
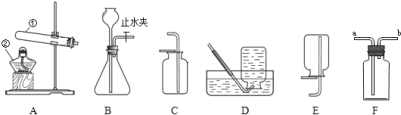
(3)实验室常用氯化铵固体与碱石灰固体共热来制取氨气(NH3)。常温下氨气(NH3)是一种无色、有刺激性气味的气体,密度比空气小,氨气(NH3)极易溶于水。制取并收集氨气(NH3),应该从图中选择的发生装置是______,收集装置是______。
【答案】 Ⅱ Ⅲ 对比氧化铁和二氧化锰对过氧化氢的催化效果 二氧化锰对过氧化氢的催化效果更好 催化剂可以加快化学反应速率 催化剂不能改变生成物的量 B A E
Ⅱ Ⅲ 对比氧化铁和二氧化锰对过氧化氢的催化效果 二氧化锰对过氧化氢的催化效果更好 催化剂可以加快化学反应速率 催化剂不能改变生成物的量 B A E
【解析】
过氧化氢在二氧化锰催化作用下生成水和氧气,氧气具有助燃性,能使带火星的木条复燃。
[实验原理]实验室用过氧化氢溶液制取氧气的反应为过氧化氢在二氧化锰催化作用下生成水和氧气,反应的符号表达式为 .
.
[实验结论] 实验Ⅱ、Ⅲ中均有ag的氧化铁,故实验Ⅱ、Ⅲ分别证明氧化铁的化学性质和质量在反应前后均没有发生变化,可以作过氧化氢分解的催化剂。
[实验评价]
(1)分别量取5mL15%过氧化氢溶液放入C、D两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,故实验设计Ⅳ的目的是对比氧化铁和二氧化锰对过氧化氢的催化效果。
(2)若实验Ⅳ观察到D试管中产生气泡的速率更快,可以得到的结论是二氧化锰对过氧化氢的催化效果更好。
[实验拓展]
由实验数据可知,结论是催化剂可以加快化学反应速率、催化剂不能改变生成物的量。
(2)A、MnO2能作过氧化氢溶液分解的催化剂,也可以作氯酸钾的催化剂,故A不正确;
B、同一个化学反应可以有多种催化剂,故B正确;
C、催化剂能加快或抑制化学反应的速率,故C不正确;
D、用作催化剂的物质可能是其他反应的反应物或生成物,故D不正确。故选B。
(3)实验室常用氯化铵固体与碱石灰固体共热来制取氨气(NH3),故应该从图中选择的发生装置是A,常温下氨气(NH3)是一种无色、有刺激性气味的气体,密度比空气小,氨气(NH3)极易溶于水,用向下排空气法收集,故收集装置是E。

 阅读快车系列答案
阅读快车系列答案【题目】某兴趣小组的同学为测定某石灰石中碳酸钙(假设:石灰石中的杂质不与盐酸反应)的质量分数,称取一定质量的石灰石置于烧杯中,用某浓度的稀盐酸100g,分5次加入,每次充分反应后,取出固体,经过滤、洗涤、干燥等操作后称重,各次稀盐酸用量和剩余固体质量记录如下:
实验次数 | 稀盐酸的用量(g) | 剩余固体的质量(g) |
① | 20 | 16.25 |
② | 40 | 12.50 |
③ | 60 | m |
④ | 80 | 5.00 |
⑤ | 100 | n |
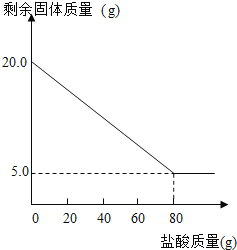
请细心观察表格和图像,回答下列问题:
(1)第_____次石灰石中的碳酸钙与盐酸恰好反应完毕。
(2)表格中m=_____g,n=_____g。
(3)计算该石灰石样品中碳酸钙的质量分数_____。
(4)计算该石灰石样品完全反应生成二氧化碳的质量_____。
【题目】小金同学分别用向上排空气法和排水法各收集一瓶氧气,然后进行铁丝燃烧的实验,发现燃烧现象不同,于是对铁丝燃烧与氧气浓度的关系进行了探究。
(进行实验)取5根相同的铁丝(直径0.6mm),卷成相同的螺旋状后,分别在氧气体积分数不同集气瓶中进行实验,实验记录如下
实验次数 | 氧气的体积分数% | 实验现象 |
第一次 | 90% | 燃烧剧烈,火星四射,燃烧时间长,实验成功 |
第二次 | 80% | 燃烧现象与90%的相比没有明显差异,实验成功 |
第三次 | 70% | 燃烧比80%的弱,燃烧时间比80%的短,实验成功 |
第四次 | 60% | 燃烧比70%的弱,燃烧时间更短,实验成功 |
第五次 | 50% | 铁丝没有燃烧 |
(1)铁丝燃烧的文字表达式为_________
(2)通过这组探究实验,可得出的结论________。
(3)要研究铁丝的粗细对燃烧现象的影响,下列实验能达到目的是_______。
A 在同一瓶氧气中,先后进行不同粗、细铁丝的燃烧实验
B 在两瓶不同浓度的氧气中,分别同时进行粗、细铁丝的燃烧实验
C 在两瓶相同浓度的氧气中,分别进行粗、细铁丝的燃烧实验
(反思与评价)对氧气纯度要求较高的实验应采取_____收集氧气。