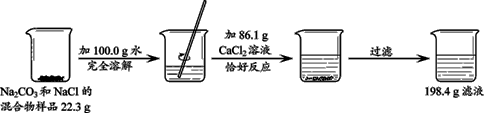题目内容
(3分)
将碳酸钠和硫酸钠的固体混合物6g放入烧杯中,此时总质量为106g,加入24.5g硫酸,恰好完全反应(反应方程式为Na2CO3 + H2SO4 ="=" Na2SO4 + H2O +CO2↑),待没有气泡逸出后再次称量,总质量为 128.3g。计算所得溶液中溶质的质量分数(CO2的溶解忽略不计)
将碳酸钠和硫酸钠的固体混合物6g放入烧杯中,此时总质量为106g,加入24.5g硫酸,恰好完全反应(反应方程式为Na2CO3 + H2SO4 ="=" Na2SO4 + H2O +CO2↑),待没有气泡逸出后再次称量,总质量为 128.3g。计算所得溶液中溶质的质量分数(CO2的溶解忽略不计)
27.6%
反应生成的CO2质量为:106g +24.5 g -128.3 g =" 2.2" g ……………………(1分)
设生成Na2SO4质量为x,原有Na2CO3质量为y
Na2CO3 + H2SO4 =" Na2SO4" + H2O + CO2↑
106 142 44
y x 2.2g
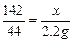 x=7.1g
x=7.1g 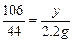 y=5.3g
y=5.3g
所得溶液中溶质的质量分数: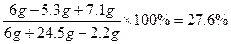 ……1分
……1分
答:所得溶液中溶质的质量分数为27.6%。(其它合理解法均可)
设生成Na2SO4质量为x,原有Na2CO3质量为y
Na2CO3 + H2SO4 =" Na2SO4" + H2O + CO2↑
106 142 44
y x 2.2g
|
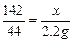 x=7.1g
x=7.1g 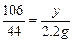 y=5.3g
y=5.3g所得溶液中溶质的质量分数:
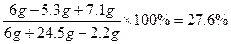 ……1分
……1分答:所得溶液中溶质的质量分数为27.6%。(其它合理解法均可)

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 CaCO3↓ + 2NaCl
CaCO3↓ + 2NaCl