题目内容
随着人们对酒驾危害认识的加深,司法机关对于酒驾、醉驾的处罚将日趋加重。醉酒的原因是酒中含有的乙醇对人的神经系统有刺激作用。交警对呼气酒精检验的原理是:橙色的K2Cr2O7酸性溶液遇乙醇会迅速变成蓝绿色。
白酒是乙醇的水溶液,酒中的乙醇在微生物作用下能被氧化成乙酸。小刚家有一瓶密封存放的白酒,他想知道该白酒的组成情况,于是进行如下实验探究:
【提出问题】该白酒中的溶质主要有哪些?
【查阅资料】材料一:乙醇(C2H5OH),俗称酒精,易溶于水,水溶液呈中性。在加热条件下,可以把氧化铜还原为单质铜。
材料二:乙酸(CH3COOH),又名醋酸,易溶于水,具有酸的通性。
【提出猜想】猜想1:只有乙醇
猜想2:只有乙酸
猜想3:
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量白酒于试管中,滴入几滴橙色的K2Cr2O7酸性溶液 | | 猜想1成立 |
| ② | |
【实验反思】操作①能否改为“将加热后的表面有黑色氧化铜的铜丝插入盛有白酒的试管中”? ,理由是 。
【提出猜想】猜想3:既有乙醇,又有乙酸
【实验探究】实验操作 实验现象 实验结论 溶液呈蓝绿色 ②取少量白酒于试管中,滴入几滴紫色石蕊试液。(或取少量碳酸钠溶液于试管中,滴入适量白酒)[其他合理答案同样给分] 溶液显紫色
(没有气泡放出)
【实验反思】不能 只有乙酸也能使铜丝表面由黑色变为红色
解析试题分析:由成分可知,还可能是乙醇和乙酸的混合物;根据实验结论:猜想1成立,故只有乙醇。根据资料及乙醇的性质“橙色的K2Cr2O7酸性溶液遇乙醇会迅速变成蓝绿色”可知溶液呈蓝绿色;在通过乙酸的性质证明没有乙酸即可;由于乙酸呈酸性,能与氧化铜反应,故也能使铜丝表面由黑色变为红色。
考点:酒精

 名校课堂系列答案
名校课堂系列答案在化学课上,甲同学将燃烧的钠迅速伸入到盛有CO2的集气瓶中,钠在其中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上附粘附着白色物质。
【提出问题】黑色颗粒和白色物质是什么?
【进行猜想】甲认为黑色颗粒是 ,白色物质可能是Na2O或 ;
乙同学还认为白色物质是氢氧化钠。
甲同学立刻认为乙同学的猜想是错误的,其理由是 。
【查阅资料】氧化钠为白色粉末,溶于水生成氢氧化钠:Na2O + H2O = 2NaOH
【实验探究】甲同学对白色物质进行实验探究。
| 实验方案 | 实 验 操 作 | 实验现象 | 结 论 |
| 方案1 | 取样品少量于试管中,加入适量水,振荡,样品 全部溶于水,向其中加入无色酚酞试液 | 溶液变成红色 | 白色物质 为Na2O |
| 方案2 | ①取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的CaCl2溶液 | 出现白色沉淀 | 白色物质 是 |
| ②静置片刻,取上层清液于试管中,滴加无色酚酞试液 | 无明显现象 |
【得出结论】钠在二氧化碳中燃烧的化学方程式为 。
① ,
② 。
实验室有一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样。已知它是无色液体,是初中化学常用的试剂。小强和小华同学很感兴趣,决定对其成分进行探究:
【提出问题】这瓶试剂可能是什么溶液呢?
【交流讨论】根据受损标签的情况判断,这瓶试剂不可能是 。
A.酸 B.碱 C.盐
【查阅资料】
Ⅰ.初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3。
Ⅱ. Na2CO3和NaHCO3溶液都呈碱性。
Ⅲ.测定室温(20℃)时,四种物质的溶解度的数据如下:
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度/g | 36 | 109 | 215 | 9.6 |
【得出结论】小华根据试剂瓶标注的溶质质量分数10%和上表中的溶解度的数据判断,
这瓶试剂不可能是 。
【作出猜想】①可能是 溶液;②可能是Na2CO3溶液;③可能是NaCl。
【设计并实验】
(1)小强用洁净的玻璃棒蘸取该溶液滴在pH试纸上,测得pH>7,这瓶试剂不可能
是 。
(2)小强为了检验该溶液是NaOH溶液还是Na2CO3溶液,他又进行了如下实验:
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中, 滴加氢氧化钙溶液 | | 猜想②正确 相关的化学方程式 |
某化学兴趣小组在做完制取二氧化碳的实验后(用石灰石与稀盐酸制取),对反应后反应器中剩余溶液的溶质成分产生了兴趣。他们继续进行了如下实验探究。
【分析推断】根据制取二氧化碳的反应原理,可以确定剩余溶液中一定含有氯化钙,但其中是否含有氯化氢需要通过实验来证明。若剩余溶液显酸性(含有
H+),说明含有氯化氢。
【查阅资料】碳酸钙不溶于水,氯化钙溶液不显酸性。
【实验过程】
将剩余溶液倒入烧杯中,微热后冷却至室温。
| | 实验操作 | 实验现象 | 实验结论 |
| 甲同学 | 取烧杯中溶液少许于试管中,向其中滴加 | 现象:溶液变为红色 | 溶液显酸性(含有H+),溶质中有氯化氢 |
| 乙同学 | 取烧杯中溶液少许于试管中,向其中加入少量锌粒 | 现象: 反应的化学方程式是: | |
| 丙同学 | 取烧杯中溶液少许于试管中,向其中加入少量石灰石 | 现象: |
【拓展提高】若要从剩余溶液中得到尽可能多的纯净的氯化钙固体,同学们认为可以向剩余溶液中加入稍过量的 (填化学式),经 ,蒸发等操作后即可完成。
一次性塑料包装袋造成的环境污染已经引起社会的高度关注,许多城市已经开始推广使用纸制食品袋。同学们经查阅资料得知,纸袋的组成成分中一定含有碳元素和氢元素,可能含有氧元素,于是他们利用以下装置进行实验测定。请回答下列问题: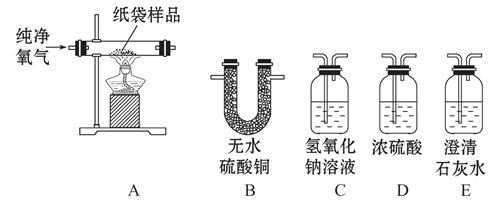
(1)实验中C装置内发生反应的化学方程式为 。
(2)实验中选择纯净的氧气而不用空气的原因是 。
(3)为分别吸收纸袋充分燃烧的产物,并通过清晰可见的现象检验吸收是否安全高效,以上实验装置正确的连接顺序是A→( )→( )→( )→( )(填写装置的字母代号)
(4)将实验装置正确连接之后,确认气密性良好,充分燃烧16.2 g纸袋样品,测得相关实验数据见表(假定燃烧产物被完全吸收,灰烬质量忽略不计)
| 装置 | 实验前装置的质量 | 实验后装置的质量 |
| B | 200.0 g | 200.0 g |
| C | 210.0 g | 234.2 g |
| D | 220.0 g | 229.0 g |
| E | 210.0 g | 212.2 g |
通过分析和计算可推断得出,纸袋样品中 (填“含”或“不含”)氧元素,其碳、氢两种元素的原子个数的最简整数比为 。