��Ŀ����
����Ŀ��ijƷ�ƴ����к��������Ȼ��ơ�ij��ѧ̽��С��Ϊ�˲ⶨ�ô���Ĵ��ȣ���������ʵ�飺
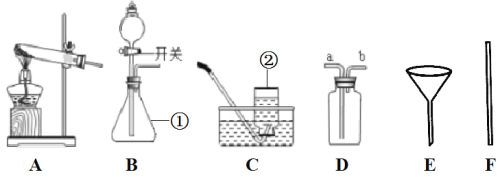
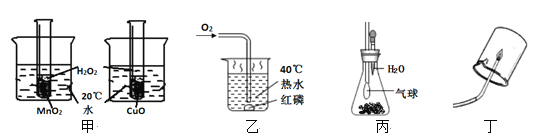
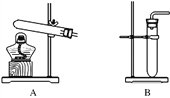
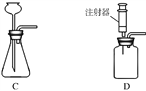
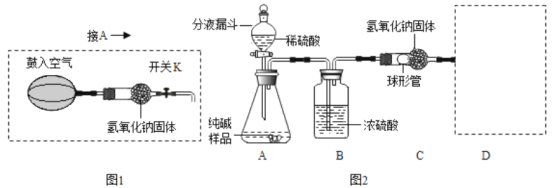
�����ʵ�鷽����ʵ��װ��(��ͼ2��ʾ���̶�װ����ȥ)��
��Ҫ�ⶨ��ʵ�����ݣ�������Ʒ��������ʵ��ǰ����Cװ��(�����������ƹ���)��������
(1)Aװ���з�Ӧ��ѧ����ʽ��________��Ϊ�˱�֤������Ʒ�е�̼������ȫ��Ӧ���������_______��
(2)Bװ�õ�������______��Cװ�õĻ�ѧ����ʽ��_____________��
(3)����D__________(��Ҫ������װ��ʾ��ͼ)��
����������
(4)��ͬѧ��Ϊͼ2��ʾʵ��װ�û���ɲ�ô���Ĵ���ƫ�ͣ�ԭ����_____________________��
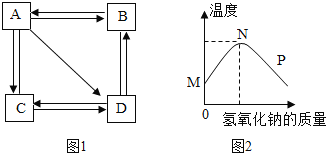
(5)Ϊ�˿˷�ͼ2װ�õIJ��㣬��ͬѧ�������Ӧ����ͼ1װ����Aװ������ (Aװ����ԭ˫������������������)���ڷ�Ӧǰ������ͼ1װ�÷����λ������������
�ٷ�Ӧǰ���Ͽ�B��Cװ��֮������ӣ���ͼ1װ��������������_______________��
�ڷ�Ӧ����ͼ1װ��������������_________________��
����Aװ���еķ�Ӧ����ʱ������K���ڹر�״̬����ԭ����____________��
�����ݴ�����
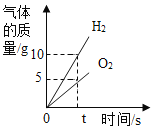
(6)�Ƶô�����Ʒ������Ϊ10.8g��ʵ��ǰ����Cװ�õ��������ֱ�Ϊ75.2g�� 79.6g������Ĵ���Ϊ_______% (����������С�����1λ)��
����˼�����ۣ�
(7)�ܷ���ϡ�������ϡ���ͬѧ�Ǿ���������Ϊ���ܣ�������___________��
(8)�Ľ����ʵ��װ���ܼ��ٲⶨ����ԭ���Ǣٷ�Ӧ���ɵ�CO2�����ܱ�װ��C���գ���_________��
���𰸡�Na2CO3+H2SO4=Na2SO4+H2O+CO2�� ��ε���ϡ���������ٲ��� ����Ϊֹ ��ȥˮ���� 2NaOH+CO2= Na2CO3+H2O װ�������ƹ�������ι� ABװ���в�����Ӧ�����Ķ�����̼����δ��C�е������������� �ò���������̼�Ŀ����ų�ABװ����ԭ�еĿ��� �ò���������̼�Ŀ����ų�������ABװ���з�Ӧ�����Ķ�����̼���� ����ͼ1װ�����շ�Ӧ�����IJ��ֶ�����̼���� 98.1 ϡ����ӷ����Ȼ������壬��Cװ�����գ�Ӱ��ʵ��ⶨ ����ABװ����ԭ�������ж�����̼�����ʵ��ĸ���
��������
(1)������Ҫ�ɷ���̼���ƣ�̼���ƺ����ᷴӦ���������ơ�ˮ�Ͷ�����̼����ѧ����ʽΪ�� Na2CO3+H2SO4=Na2SO4+H2O+CO2������Ϊ�÷�Ӧ�����ݲ�������ε���ϡ���������ٲ��� ����Ϊֹ��û�����ݲ����ˣ�˵��̼��ط�Ӧ���ˣ�
(2)Ũ���������ˮ�ԣ�����Bװ����Ҫ�dz�ȥ������̼�е�ˮ������Cװ���еķ�Ӧ���������ƺͶ�����̼��Ӧ����̼���ƺ�ˮ����ѧ����ʽΪ��2NaOH+CO2= Na2CO3+H2O��
(3)Dװ���Ƿ�ֹ�����е�ˮ��������̼����Cװ�������������װ�������ƹ�������ιܾ��ܴﵽĿ�ģ�
(4)��Ӧ��������ABװ���л������Ӧ���ɵĶ�����̼���壬δ��C�е������������գ����¶�����̼�������٣������ƫС��
(5)�ٹ���Ŀ����������������ƣ������ѿ����ж�����̼��ȥ���ò������� ��̼�Ŀ����ų�ABװ����ԭ�еĿ���������ԭ�еĿ����к��ж�����̼��
���ò���������̼�Ŀ����ų�������A��Bװ���з�Ӧ�����Ķ�����̼���壬ʹ��Ӧ�����Ķ�����̼ȫ����Cװ�����գ�
����������ڹر�״̬�����ɵĶ�����̼�����ͼ1�У���ͼ1�������������գ�
(6)��Ӧǰ��Cװ���������������������ɶ�����̼���������������ɶ�����̼������Ϊ��79.6g- 75.2g=4.4g��������4.4g ������̼��Ҫ̼���Ƶ�����Ϊx��
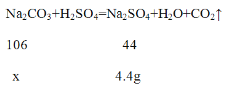
![]() =
=![]() �����x= 10.6g
�����x= 10.6g
���Դ���Ĵ���Ϊ��![]() ��100%=98.1%��
��100%=98.1%��
(7)������ϡ�������ϡ����ϡ������ӷ����Ȼ������壬��Cװ�����գ�Ӱ��ʵ��ⶨ��
(8)�Ľ���װ�õ��ŵ��У���Ӧ���ɵ�CO2�����ܱ�Cװ�����գ�����A��Bװ����ԭ�������еĶ�����̼�����ʵ��ĸ��š�