题目内容
【题目】用化学用语填写
①两个氢原子_____;②铵根离子_____;③3个铝离子_____;
④氢氧化钠_____;⑤硫酸亚铁_____;⑥氧化镁中镁显+2价_____。
【答案】2H NH4+ 3Al3+ NaOH FeSO4 ![]()
【解析】
①两个氢原子就是在氢元素符号的前面加上数字2,故填:2H
②铵根离子带有一个单位的正电荷,故填:NH4+
③3个铝离子就是在铝离子的前面加上数字3,故填:3Al3+
④氢氧化钠中钠元素为+1价,氢氧根为﹣1价,其化学式为NaOH,故填:NaOH
⑤硫酸亚铁中铁元素为+2价,硫酸根为﹣2价,其化学式为FeSO4 ,故填:FeSO4
⑥氧化镁中镁显+2价就是在氧化镁化学式中镁元素符号的正上方加上+2,故填:![]()

【题目】钙片的标签如图所示,且知此钙片成分中只有碳酸钙中含有钙元素,此标签中的含钙量是否正确?
(1)______(填“正确”或“错误”),为测定其含钙量,小东每次取10片钙片放入已称量的含足量稀盐酸的烧杯中,充分反应后再称取烧杯和剩余物的总质量,小东做了三次实验数据如下:
物质的质量 | 第1次 | 第2次 | 第3次 | 平均值 |
反应前:烧杯+稀盐酸 | 22g | 22g | 22g | 22g |
10片钙片 | 8g | 8g | 8g | 8g |
反应后:烧杯+稀盐酸 | 26.7g | 26.5g | 26.9g | 26.7g |
(2)每片钙片中含碳酸钙质量是____g
(3)通过小东的实验,你建议厂家如何修改标签?______。

【题目】化学是造福人类的科学,请利用所学知识回答下列问题。
(1)新型材料有着广泛的应用。
应用 | “蛟龙”号深潜器 | “神舟”五号宇航员航天服 | 新型水处理剂 |
用到的材料 | 特种钢 | 高强度涤纶 | 纳米铁粉 |
①上述材料中属于有机合成材料的是______。
②纳米铁粉能吸附废水中的某些污染物,被吸附后的废水经沉降、过滤可去除污染物。
下列物质也能因吸附而具有净水作用的是______(填字母)
a.生石灰 b.活性炭 c.纯碱
(2)溶液与人们的生产生活密切相关,图I为甲、乙、丙三种固体物质的溶解度曲线。
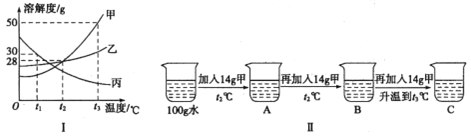
①t1℃时甲、乙、丙三种物质的溶解度由大到小的顺序是______。
②某同学按图Ⅱ所示进行实验,得到相应温度下的A、B、C三种溶液,其中属于饱和溶液的是______(填字母)。
③t3℃时向盛有40g甲物质的烧杯中加入50g水充分溶解后,所得溶液溶质的质量分数为______。(结果精确到0.1%)
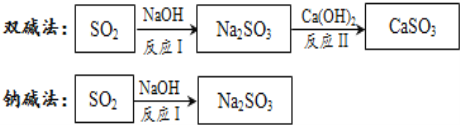
【题目】工业烟气通常含二氧化硫,在排放前需经脱硫处理![]() 如图是两种常用脱硫工艺中含硫物质的转化路径
如图是两种常用脱硫工艺中含硫物质的转化路径![]() 部分产物已略
部分产物已略![]() .
.
(1)下列环境问题与![]() 有关的是 ______
有关的是 ______ ![]() 填字母序号
填字母序号![]() .
.
A酸雨 B温室效应 C臭氧空洞
(2)双碱法中的“双碱”指的是 ______![]() 填化学式
填化学式![]() .
.
(3)写出反应Ⅰ的化学方程式: ______ .
(4)反应Ⅱ所属的基本反应类型是 ______ .
(5)已知部分原料的价格如下表所示.
试剂 | Ca(OH)2 | NaOH |
价格(元/kg) | 0.36 | 2.90 |
两种工艺中,处理相同量的SO2,双碱法所需的原料成本更低,原因是______![]() 物质组成和变化分析
物质组成和变化分析![]() .
.
【题目】兴趣小组的同学学习了碳酸钠的性质后,对碳酸氢钠的性质也进行探究。
(问题1)碳酸氢钠溶液与碳酸钠溶液的酸碱性
(实验1)用pH试纸测定等浓度的碳酸氢钠和碳酸钠溶液的pH,分别为9和12;
(结论1)两种溶液都呈碱性,它们的碱性强弱顺序为_____。
(问题2)碳酸氢钠溶液、碳酸钠溶液与酸的反应
(实验2)等浓度的碳酸氢钠和碳酸钠溶液分别与相同浓度的盐酸反应
操作和现象如下表:
序号 | 操作 | 现象 |
实验① | 碳酸氢钠溶液逐滴加入盐酸中 | 立刻产生气泡 |
实验② | 碳酸钠溶液逐滴加入盐酸中 | 立刻产生气泡 |
实验③ | 盐酸逐滴加入碳酸氢钠溶液中 | 立刻产生气泡 |
实验④ | 盐酸逐滴加入中碳酸钠溶液中 | 滴加一会后才有气泡产生 |
(问题3)实验④与另外三个实验现象不同的原因
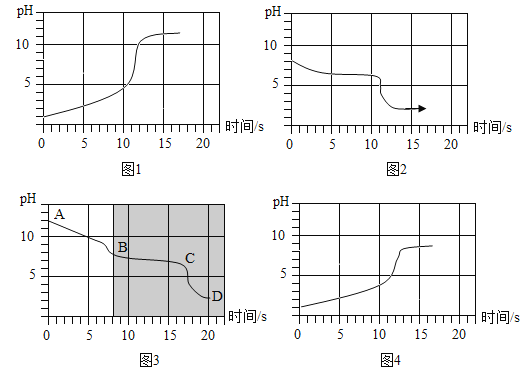
(实验3)将等浓度的碳酸氢钠和碳酸钠溶液与相同浓度的盐酸互滴,利用手持传感器测定反应中溶液pH变化,四个实验的pH变化与时间的关系如图所示。
(分析)
(1)如图表示的实验是_____(填实验2中的序号)。
(2)比较如图与如图发现:如图中的阴影部分与如图叠合后,图象基本重合。
则如图中的AB段发生反应的化学方程式为_____,BC段发生反应的化学方程式为_____,D点的溶质为_____(写化学式);所以,“盐酸逐滴加入碳酸钠溶液中,滴加一会后才有气泡产生”的原因是_____。
(3)比较如图与如图发现:不同的操作有不同现象,试分析造成这一现象的原因:_____。
(应用)
用稀盐酸来鉴别一瓶溶液是氢氧化钠还是碳酸钠时,应如何操作? _____。