题目内容
【题目】根据题意回答。
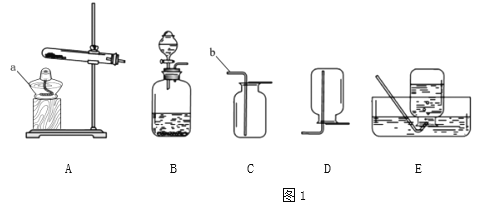
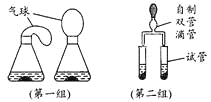
①写出仪器名称:a_______,b_______;
②实验室用氯酸钾和二氧化锰的混合物制取氧气,可选择的一组装置是_______(填编号)写出反应的化学方程式_______;
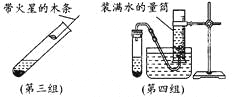
③下图是检查装置气密性的过程。最终在F处观察到的现象是_______(选填“甲~丁”);

④ 资料表明:高铁酸钾(K2FeO4)固体也能用于制取氧气,原理如下:
方案一:4K2FeO4![]() 2Fe2O3+4K2O+3O2↑
2Fe2O3+4K2O+3O2↑
方案二:4K2FeO4+10H2O→4Fe(OH)3↓+8KOH+3O2↑
Ⅰ.关于以上方案说法错误的是_______
a.方案一是分解反应
b.方案二更节能简便
c.方案一、二均可在图1的装置B中进行实验
d.制取等质量的氧气,两种方案所需高铁酸钾的质量相等
Ⅱ.若用方案一(4K2FeO4![]() 2Fe2O3+4K2O+3O2↑)制取0.3mol氧气,需要高铁酸钾的物质的量为_______ mol(根据化学方程式列式计算)。
2Fe2O3+4K2O+3O2↑)制取0.3mol氧气,需要高铁酸钾的物质的量为_______ mol(根据化学方程式列式计算)。
【答案】酒精灯导管AC2KClO3![]() 2KCl+3O2↑丙c设需高铁酸钾的物质的量为x mol
2KCl+3O2↑丙c设需高铁酸钾的物质的量为x mol
4K2FeO4![]() 2Fe2O3+4K2O+3O2↑
2Fe2O3+4K2O+3O2↑
4 3
x 0.3
x = 0.4(mol)
答:需高铁酸钾的物质的量为0.4mol。
【解析】②选择发生装置需考虑是因素是,反应物的状态和反应条件。加热固体制取气体,发生装置为A,固体和液体常温下反应制取气体应选用的发生装置为B。选择收集装置需考虑气体的密度,是否与空气的成分反应,气体在水中的溶解性。氧气的密度比空气的大,可以用向上排空气法收集,氧气难溶于水可以用排水法收集。实验室用氯酸钾和二氧化锰的混合物制取氧气,可选择的一组装置是AC或AE;反应的化学方程式2KClO3![]() 2KCl+3O2↑;③检查装置的气密性,组装好仪器,将导管放入水中,用手握试管,导管口有气泡冒出,或松开手,试管冷却至室温后,试管内形成一段液柱,证明装置的气密性好;④Ⅰ.由一种物质生成两种或两种以上物质的反应叫分解反应;方案二常温下进行,更节能简便方案二固液常温,在装置B内进行,方案一在A中进行;两个方案中高铁酸钾与氧气的质量比相同,所以制取等质量的氧气,两种方案所需高铁酸钾的质量相等;Ⅱ. 设需高铁酸钾的物质的量为x mol
2KCl+3O2↑;③检查装置的气密性,组装好仪器,将导管放入水中,用手握试管,导管口有气泡冒出,或松开手,试管冷却至室温后,试管内形成一段液柱,证明装置的气密性好;④Ⅰ.由一种物质生成两种或两种以上物质的反应叫分解反应;方案二常温下进行,更节能简便方案二固液常温,在装置B内进行,方案一在A中进行;两个方案中高铁酸钾与氧气的质量比相同,所以制取等质量的氧气,两种方案所需高铁酸钾的质量相等;Ⅱ. 设需高铁酸钾的物质的量为x mol
4K2FeO4![]() 2Fe2O3+4K2O+3O2↑
2Fe2O3+4K2O+3O2↑
4 3
x 0.3
x = 0.4(mol)
答:需高铁酸钾的物质的量为0.4mol。

 教材全解字词句篇系列答案
教材全解字词句篇系列答案