题目内容
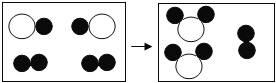
【题目】请结合图示实验装置,回答下列问题:
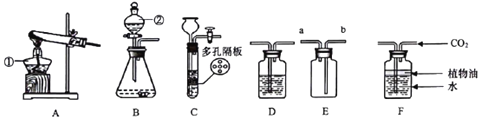
(1)写出仪器的名称①_____ ②__________________
(2)用高锰酸钾制氧气选用的发生装置是______(选填序号),反应的化学方程式为______。
(3)若B装置中固体为锌粒,②中加入______试剂可制得氢气,要获得干燥的氢气,应先将气体通过盛有______的D装置,再用E装置收集,气体应端通入______(选填“a”或“b”)。
(4)实验室可用B或C装置制取二氧化碳,反应的化学方程式为______,C相对于B装置的优点有______
(5)若用F装置收集二氧化碳,植物油的作用是______。
【答案】酒精灯 分液漏斗 A 2KMnO4 ![]() K2MnO4+MnO2+O2↑ 稀硫酸 浓硫酸 a CaCO3+2HCl=CaCl2+H2O+CO2↑ 能够随时使反应进行或停止 防止二氧化碳溶于水
K2MnO4+MnO2+O2↑ 稀硫酸 浓硫酸 a CaCO3+2HCl=CaCl2+H2O+CO2↑ 能够随时使反应进行或停止 防止二氧化碳溶于水
【解析】
(1)写出仪器①的名称是酒精灯,故填酒精灯;
写出仪器②的名称是分液漏斗,故填分液漏斗。
(2)用高锰酸钾制氧气是加热固体生成气体的反应,发生装置应选择固体受热发生装置,故选A;
高锰酸钾受热反应生成锰酸钾、二氧化锰和氧气,故化学方程式写为:2KMnO4 ![]() K2MnO4+MnO2+O2↑。
K2MnO4+MnO2+O2↑。
(3)实验室中一般用锌和稀硫酸反应制取氢气,故填稀硫酸;
浓硫酸具有吸水性,常用作干燥剂来干燥气体,故填浓硫酸;
氢气的密度小于空气的密度,氢气应从短管进入瓶中,故选a。
(4)实验室用石灰石和稀盐酸反应来制取二氧化碳,反应的化学方程式写为CaCO3+2HCl=CaCl2+H2O+CO2↑;
C装置可以通过开关的开闭来控制反应的进行或停止,故填能够随时使反应进行或停止;
(5)在水上覆盖一层植物油可以防止二氧化碳溶于水,故填防止二氧化碳溶于水。

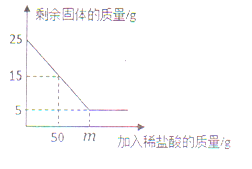
【题目】某研究学习小组欲测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品20g,把80g稀盐酸分四次加入,实验过程所得数据如下表(已知石灰石样品中含有的二氧化硅等杂志不溶于水,不与稀盐酸反应)。根据实验数据计算:
实验次数 | 加入稀盐酸的质量/g | 剩余固体的质量/g |
1 | 20 | 15 |
2 | 20 | 10 |
3 | 20 | 6.8 |
4 | 20 | 6.8 |
(1)样品中碳酸钙的质量分数是______。
(2)计算样品中碳酸钙完全反应时生成的二氧化碳的质量_____。