题目内容
【题目】如图是某些气体的微观示意图,图中“〇”和“●”分别表示不同的原子
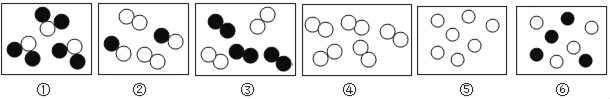
(1)其中表示纯净物的有_____(填序号)能表示氢气和氧气的混合气体的是_____能表示氦气和氖气的混合气体的是_____,能表示氮气的是_____
(2)由图③所示物质转化为图①所示物质可表示我们已经学过的一个重要化学变化,该反应的符号表达式为_____
【答案】①④⑤ ③ ⑥ ④ 2H2+O2 ![]() 2H2O
2H2O
【解析】
(1)由微粒的构成可知,其中①④⑤表示的物质是由同种的分子构成的,属于纯净物;③表示的物质是由两种分子构成的,每种分子是由同种的两个原子构成的,能表示氢气和氧气的混合气体;⑥表示的物质是两种,每种物质都是由原子直接构成的,能表示氦气和氖气的混合气;④表示的物质是由同种分子构成的,每个分子是由两个原子构成,能表示氮气
(2)由微粒的构成及微粒的变化数目关系可知,氢气燃烧生成水的反应,能表示由图③所示物质转化为图①所示物质,该反应的化学方程式为:2H2+O2 ![]() 2H2O。
2H2O。

 寒假学与练系列答案
寒假学与练系列答案【题目】酸、碱、盐在生产生活中具有广泛的用途。
化学实验室有失去标签的稀硫酸、氢氧化钠、氢氧化钙、碳酸钠、氯化钡五瓶无色溶液,现将其任意编号:A、B、C、D、E,然后两两组合进行实验,其部分现象如下表(微溶物视为可溶物):
实验 | A+C | B+C | A+B | A+D |
现象 | 产生沉淀 | 产生沉淀 | 产生气体 | 产生沉淀 |
(1)写出溶液A、C、D中溶质的化学式A______,C______,D______。
(2)写出溶液A与D反应的化学方程式______。
(3)写出溶液A与C反应的化学方程式______。
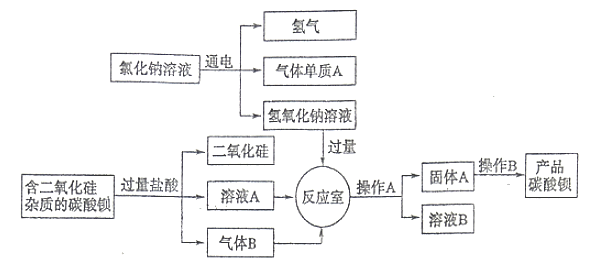
【题目】稀土金属因其独特的性能而被誉为“新材料之母”。稀土金属钇的氧化物(Y2O3)广泛应用于航空航天涂层材料,其颗粒大小决定了产品的质量。利用富钇稀土(含Y2O3约70%,含Fe2O3、CuO、SiO2等约30%)生产大颗粒氧化钇的种工艺如下:
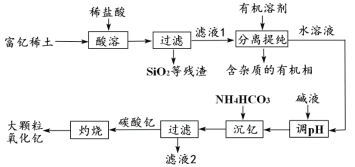
(1)氧化钇(Y2O3)中,Y元素的化合价为____________。
(2)“酸溶”过程中,氧化钇与盐酸反应的化学方程式是______________________________。
(3)“分离提纯”是为了除去滤液1中的_____________________________(填化学式)。
(4)“调pH”时加入碱液使溶液的pH_____________(填“增大”或“减小”)。
(5)碳酸钇灼烧分解的化学方程式是_______________________________________。
(6)为了获得大颗粒氧化钇,某小组研究了条件对产品直径的影响,相关数据如下(D50表示颗粒直径):
实验编号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
沉淀反应温度/℃ | 60 | 80 | 85 | 93 | 93 | 93 |
料液浓度Kg/L | 30 | 30 | 30 | 30 | 40 | 40 |
灼烧温度/℃ | 1100 | 1100 | 1100 | 1100 | 1100 | 1400 |
氧化钇D50/um | 6.00 | 21.65 | 35.99 | 38.56 | 35.99 | 61.54 |
分析上表数据,其他条件不变时,若将灼烧温度均升高至1400℃,预期所得氧化钇D50最大的是____________(填实验编号)。
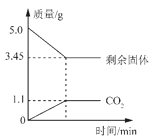
【题目】我市石灰石资源丰富,某课外小组同学为了测定石灰石中碳酸钙的质量分数,取某地石灰石样品10.0g于烧杯中,将100g稀盐酸分5次加入烧杯中,充分反应后(杂质不与稀盐酸反应),测得剩余固体的质量记录如下.
次数 | 1 | 2 | 3 | 4 | 5 |
加入稀盐酸质量/g | 20 | 20 | 20 | 20 | 20 |
剩余固体质量/g | 8.0 | 6.0 | 4.0 | 2.5 | X |
请计算:(1)X的值为__________.
(2)该石灰石样品中碳酸钙的质量分数为_____________
(3)所用稀盐酸溶质的质量分数为________.(写出计算过程)