题目内容
【题目】根据下列实验装置图回答问题:
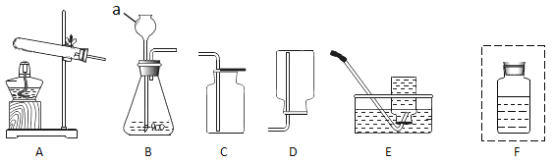
(1)甲烷是一种无色无味的气体,密度比空气小,难溶于水,实验室常采用加热无水醋酸钠和碱石灰制取甲烷,要制取一瓶较干燥的甲烷气体,最好选用的一套装置为______________(填序 号)。图中仪器a可随时向容器内添加液体药品,它的名称为________________。
(2)实验室可用 A装置制取氧气,写出其制取氧气的化学方程式_______________。 检验该气体的方法为____________。
(3)B装置可用来制取氢气,其反应的化学方程式为____________,若 用 F装置来收集氢气,请在 F处方框中将装置图补充完整_________(画出导气管及气体流入方向)。
【答案】AC 长颈漏斗 )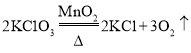 用一根带火星的木条伸入集气瓶中,木条复燃。 或 用一根燃着的木条伸入集气瓶中,木条燃烧更旺
用一根带火星的木条伸入集气瓶中,木条复燃。 或 用一根燃着的木条伸入集气瓶中,木条燃烧更旺 ![]() 等合理即可
等合理即可 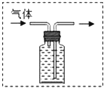
【解析】
(1)由题可知,甲烷的发生装置属于固固加热型装置,故发生装置选A,甲烷难溶于水,密度比空气的密度小,故可以选排水法或向上排空气法收集,排水法收集的气体较纯,向上排空气法收集的气体较干燥,故组合装置为:AC。仪器a的名称是长颈漏斗。
(2)装置A属于固固加热型装置,故可以用氯酸钾反应制取氧气,反应的方程式为: 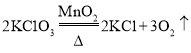 。检验氧气的方法是用一根带火星的木条伸入集气瓶中,木条复燃。 或 用一根燃着的木条伸入集气瓶中,木条燃烧更旺。
。检验氧气的方法是用一根带火星的木条伸入集气瓶中,木条复燃。 或 用一根燃着的木条伸入集气瓶中,木条燃烧更旺。
(3)锌和稀硫酸反应生成硫酸锌和氢气,可以用装置B, 反应的方程式为:![]() 。由于氢气的密度比水的密度小,故氢气由短管通入,水由长管流出,故装置图为:
。由于氢气的密度比水的密度小,故氢气由短管通入,水由长管流出,故装置图为: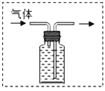 。
。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】碱式碳酸盐广泛应用于工农业生产。
(1)某碱式碳酸盐样品M(OH)2·MCO3,为确定金属M的相对原子质量,某研究小组设计如下实验装置及步骤(不考虑植物油中溶解CO2产生的影响)。
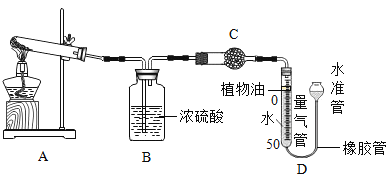
①连接装置并检查装置气密性;
②准确称量样品的质量;
③装药品,调节量气装置两边液面相平,读数;
④加热至样品质量不再减少;
⑤冷却到室温;
⑥________(请将实验步骤补充完整),读数、列式计算。
(2)装置B中的试剂是_________(填字母序号),其作用是________,C中的试剂是________(填字母序号),其作用是________。
a碱石灰 b浓硫酸 c硫酸铜
(3)步骤⑥中调节液面相平的操作是将水准管________(填“缓慢上移”或“缓慢下移”)。
(4)若其他操作均正确,仅因下列因素可使M相对原子质量的测定结果偏大的是________(填字母序号);
a反应前量气管水面在0刻度处,反应后俯视读数
b样品未分解完全即停止实验
c量气管中水面加一层植物油
(5)实际生产中的碱式碳酸铜可表示为Cu(OH)2·mCuCO3,某研究小组仍使用上述装置测定m的值,测得3组数据如下表所示。
组别 | 样品质量 | CO2体积 |
第1组 | 0.21 g | 22.41 mL |
第2组 | 0.21 g | 22.39 mL |
第3组 | 0.21 g | 22.40 mL |
取3组数据的值得到CO2的体积为_________mL,又知常温常压下CO2的密度为1.964 g/L,据此计算m的值。__________(写出计算m的过程)
【题目】甲乙小组按下图1、2所示实验对蜡烛的燃烧进行探究,获得了不同的实验现象。
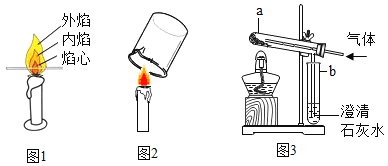
甲组:
如图1,将一根火柴梗平放入火焰中,约1s后取出,看到木条与外焰接触部分变得焦黑,与内焰接触部分为浅黑色,与焰心接触部分没有明显变化。该实验的目的是__________________,实验证明蜡烛火焰的_______________部分温度最高.
如图2,烧杯内壁有无色液滴出现,能推测蜡烛燃烧后生成了__________________。
乙组:
图2中当烧杯位置明显降低时,烧杯内壁不仅有无色液滴,还看到烧杯底部附着有黑色固体。
(提出问题)黑色固体是什么呢?
(猜想)猜想黑色固体是碳,其依据是:化学反应前后元素种类不变,并且___________________。
(实验验证)为了证明上述猜想是否正确,甲、乙小组的同学用图3装置分别设计了以下方案进行验证。
实验操作 | 实验现象 | |
甲组 | 取少量该黑色固体于a中,通入空气,点燃酒精灯加热。 | 黑色固体燃烧,发出_______________,b中溶液变浑浊。 |
乙组 | 取少量该黑色固体于a中,通入__________,点燃酒精灯加热 | 黑色固体剧烈燃烧,发出白光,b中溶液变浑浊。 |
(分析与结论)
(1)实验结束时,停止通入气体,后续两步实验操作如下,操作顺序是_____________(填字母序号)。
A熄灭酒精灯,停止加热 B将试管b移走
(2)根据甲乙两组实验b中的实验现象、都说明黑色固体燃烧生成了________________,由此可推断猜想正确。
(反思)
(1)进一步实验发现,罩在火焰上方的烧杯位置越低,产生黑色固体越多。查阅资料蜡烛主要成分是石蜡,并且:石蜡+氧气(足量)→二氧化碳+水;石蜡+氧气(少量)→一氧化碳+水;由此推测乙组实验产生黑色固体的原因是:罩在火焰上方的烧杯位置越低,蜡烛燃烧时因_________________不能及时补充,而不充分燃烧,会产生黑色固体碳。
(2)甲、乙小组最终证明了蜡烛中一定含有_____________(填字母序号)。
A碳、氢和氧三种元素 B碳和氧两种元素 C碳和氢两种元素