题目内容
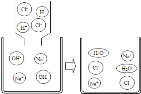
【题目】如图,A、B、C、D均为初中化学常见的物质。
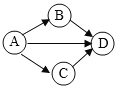
(1)如果A是一种黑色粉末,D是一种红色固体单质,C中溶质由两种元素组成,则A→C反应的化学方程式为_________________。
(2)如果A、B、C、D中都含有钠元素,B的俗名是纯碱,D是食盐的主要成分,B、C、D均为可溶的盐,D中含有两种元素,则A的化学式是_________________,B→D的化学方程式为_________________。
【答案】![]() NaOH
NaOH ![]()
【解析】
(1)A是一种黑色粉末,D是一种红色固体,可推知A是氧化铜,可以被还原成铜,因此D是铜;氧化铜还能够和酸反应,C中溶质含两种元素,因此C可以是氧化铜和盐酸反应产生的氯化铜,带入符合题意,氧化铜可以和稀盐酸反应生成氯化铜和水;故反应的方程式为:CuO+2HCl=CuCl2+H2O (其它合理答案均可);故填: CuO+2HCl=CuCl2+H2O。
(2)A、B、C、D中都含有钠元素,B的俗名是纯碱,B是碳酸钠,D是食盐的主要成分,D是氯化钠,B、C、D均为可溶的盐,D 中含有两种元素,氢氧化钠和二氧化碳反应生成碳酸钠和水,氢氧化钠和稀盐酸反应生成氯化钠和水,则A是氢氧化钠,化学式为NaOH,B→D的化学方程式为Na2CO3+BaCl2=2NaCl+BaCO3↓;故填: NaOH; Na2CO3+BaCl2=2NaCl+BaCO3↓。

【题目】同学们探究氢氧化钠与盐酸能否发生化学反应。
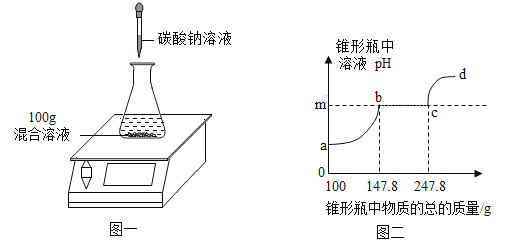
[探究活动1]同学进行了如图实验:
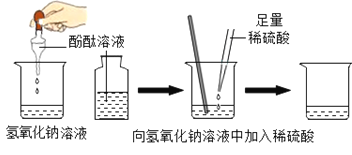
加入一定量稀盐酸后观察到溶液由红色变为无色,证明二者发生了反应。上述实验操作中有一处明显错误,请加以改正_______________。要证明稀盐酸与氢氧化钠发生了反应,除了上述方法之外,还可以按照下表实验获得结论。
实验步骤 | 实验现象 | 实验结论 |
取少量氢氧化钠溶液于试管中,加入过量稀盐酸后,再加入少量氧化铜 | ________________ | 氢氧化钠和盐酸发生了反应。加入氧化铜后发生反应的化学方程式为_____________ |
[探究活动2]如果在[探究活动1 ]中直接倾倒稀盐酸至溶液由红色变为无色,最终烧杯内的溶液中溶质的成分是什么? ( 指示剂除外)
[猜想与假设]甲猜想:氯化钠
乙猜想:_______________
甲为了证明自己的猜想,进行如下实验:
实验操作 | 实验现象 | 实验结论 |
取反应后的溶液于烧杯中,加入铁粉 | _____________ | 猜想错误 |
[探究活动3 ]中和反应能否通过判断有水生成来证明其反应发生?
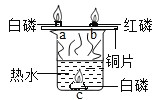
[设计实验]乙取变色硅胶、无水醋酸和氢氧化钠固体进行如图2的三个对比实验。
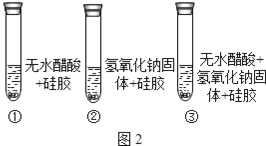
[查阅资料] a.变色硅胶吸水后由蓝色变为红色;
b.无水醋酸是一种酸,常温下为无色液体;
(1)加入试剂后.要迅速塞紧橡胶塞的原因是___________。
(2)能证明酸和碱反应有水生成的现象是___________。