题目内容
【题目】空气中氮气的含量最多,氮气在高温、高能量条件下可与某些物质发生反应。如图是以空气和其他必要的原料合成硝酸铵(NH4NO3)的工业流程。请按要求回答下列问题:
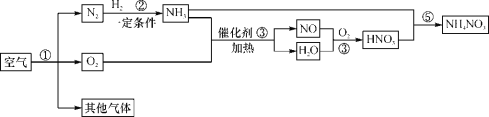
(1)步骤①中发生的是______(填“物理变化”或“化学变化”);
(2)步骤②的基本反应类型为_____;
(3)步骤③一般用五氧化二钒(V2O5)作为反应的催化剂,反应前后其质量和______都不发生改变,步骤③反应的化学方程式____(不需注明反应条件);
【答案】物理变化 化合反应 化学性质 4NH3+5O2=4NO+6H2O
【解析】
(1)利用氧气和氮气沸点的不同将二者从空气中分离,是工业上制氧气的方法,在此过程中没有生成新物质,属于物理变化,故填物理变化;
(2)步骤②是氮气和氢气在一定条件下合成氨气,属于化合反应,故填化合反应;
(3)催化剂能改变其他物质的化学反应速率,而本身的质量和化学性质不变,故填化学性质;步骤③是氨气和氧气在加热及催化剂的条件下反应生成一氧化氮和水,不需注明反应条件则方程式故填4NH3+5O2=4NO+6H2O。

 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案【题目】氯化钠是一种重要的资源,在海水中储量很丰富。
①氯化钠由______种元素组成,0.1mol 氯化钠的质量是_____g,氯化钠中氯元素的质量分数为___(精确到 0.01)。
②海水晒盐得到的粗盐中含不溶性杂质,制成精盐的操作流程如下:
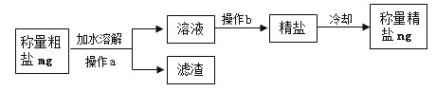
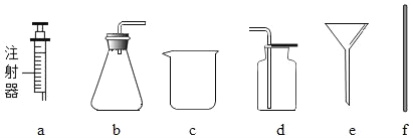
Ⅰ. 称取 mg 粗盐样品;称量时,在电子天平上放一张称量纸,然后按____键,用_______(填仪器名称),取粗盐加到称量纸上,直到天平显示 mg。
Ⅱ. 操作 a 的名称________,溶液中进一步分离获得精盐,操作 b 的名称是________。
Ⅲ. 已知:产率=(精盐的质量÷粗盐的质量)x100% 实验后各小组的产率及评价如下:
组别 | 第 1 组 | 第 2 组 | 第 3 组 | 第 4 组 | |||
产率 | 75% | 65% | 88% | 72% | |||
对产率的评价 | 偏低 | 偏低 | 偏高 | 偏低 | |||
下面是对造成产率偏高或偏低的原因分析,其中正确的是_______。
A. 第 1 组:没有蒸干,精盐中仍有水分 B. 第 2 组:过滤时滤液高于滤纸的边缘
C. 第 3 组:过滤时不小心捅破了滤纸 D. 第 4 组:食盐未溶解完就开始过滤
③若现有 25g10%的食盐溶液欲配制成 5%的食盐溶液,则需加水____g。