题目内容
【题目】(一) 实验室使用过氧化溶液与二氧化锰制取氧气并回收二氧化锰,可供选择的实验仪器和用品如下。
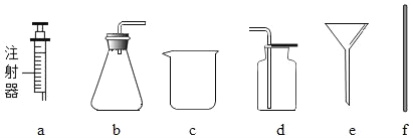
(1)仪器C的名称为_______________________。
(2)上述方法制取氧气的化学方程式_____________________________。
(3)制取氧气时,用a仪器加入过氧化氢溶液不能达到的目的是_______(填序号)。
A. 便于控制反应快慢B.定量添加药品更方便C.生成氧气质量更大
(4)回收二氧化锰时,将固液分离的操作是_______,该过程中玻璃棒的作用是______________;除图中仪器以外,过滤还需要的仪器名称是_______________。
(5)回收的二氧化锰,还可以在上述反应中反复使用。其原因是___________________________。
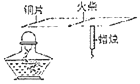
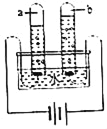
(二)某同学要探究燃烧的条件和空气中氧气的含量,进行了如下实验。(已知:白磷的着火点为![]() )
)

(1)对比步骤II和IV的现象可知,可燃物燃烧的条件之一是____________________。
(2)待装置冷却一段时间后,打开K2,如果观察到_________________________________,说明空气中氧气的体积约占1/5。若实验测得空气中氧气的体积分数小于1/5,原因可能是_______________________。(答一条即可)
【答案】烧杯 2H2O2 ![]() 2H2O+O2↑ C 过滤 引流 铁架台 反应前后二氧化锰质量和化学性质不变 可燃物的温度达到着火点 B中的水倒流回集气瓶中,量筒内剩余的水约160ml 红磷量不足或装置漏气或装置未冷却至室温就打开弹簧夹等
2H2O+O2↑ C 过滤 引流 铁架台 反应前后二氧化锰质量和化学性质不变 可燃物的温度达到着火点 B中的水倒流回集气瓶中,量筒内剩余的水约160ml 红磷量不足或装置漏气或装置未冷却至室温就打开弹簧夹等
【解析】
(一)(1)仪器C的名称为烧杯,
(2)过氧化溶液与二氧化锰制取氧气的,原理是过氧化氢在二氧化锰的作用下分解生成氧气和水,化学方程式2H2O2 ![]() 2H2O+O2↑;
2H2O+O2↑;
(3)制取氧气时,用a仪器加入过氧化氢溶液,A. 可以通过控制液体的滴加速率而控制反应快慢;B.注射器有刻度,可以控制添加药品的量;C.生成氧气质量与反应物的多少有关与容器无关,所以注射器不能改变生成物的质量,故选C;
(4)二氧化锰是难溶性固体,回收二氧化锰时,将固液分离的操作是过滤,该过程中玻璃棒的作用是引流;过滤需要的仪器有烧杯、铁架台、漏斗、玻璃棒,除图中仪器以外,还需要铁架台;
(5)回收的二氧化锰,还可以在上述反应中反复使用。其原因是二氧化锰是该反应的催化剂,反应前后质量和化学性质不变;
(二)(1)对比步骤II中可燃的白磷没有燃烧,IV中80℃的白磷燃烧,对比现象可知,可燃物燃烧的条件之一是可燃物的温度达到着火点;
(2)吹入空气时排到量筒内的水的体积为200ml,说明吹入集气瓶的空气有200ml,磷燃烧消耗氧气,待装置冷却一段时间后,打开K2,可观察到B中的水倒流回集气瓶中,量筒内剩余的水约160ml,说明氧气约40ml,空气中氧气的体积约占1/5。若实验测得空气中氧气的体积分数小于1/5,原因可能是: 红磷量不足或装置漏气或装置未冷却至室温就打开弹簧夹等。

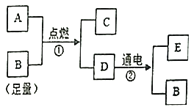
【题目】某同学进行如图实验,充分反应后,将试管①②内的物质倒入同一烧杯中混合再充分反应后过滤,结果得到滤渣A和无色滤液B。
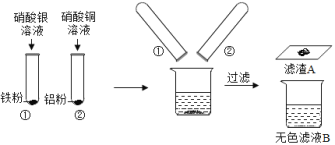
(1)试管①中反应的化学方程式为:_____;试管②中观察到的现象是:有红色固体出现,溶液_____。
(2)过滤操作中需要的玻璃仪器有:烧杯、玻璃棒和_____;无色滤液B中含有的物质是H2O和_____ (填化学式 )。
(3)设计实验探究滤渣A的成分
(提出问题)滤渣A的成分是什么?
(查阅资料)银、铜、铁、铝四种金属中,只有铝可以和氢氧化钠溶液反应,化学方程式为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑。
(作出猜想)滤渣A的成分为:
猜想Ⅰ:银、铜;猜想Ⅱ:银、铜、铁;猜想Ⅲ:_____。
(分析思考)猜想Ⅰ一定不正确,原因是_____。
(进行实验)取两份滤渣样品进行实验,请填写下列空白:
样品 | 加入试剂 | 现象 |
第一份样品 | 足量稀盐酸 | 产生气泡,固体部分溶解,溶液变_____色 |
第二份样品 | 足量氢氧化钠溶液 | 现象b |
(作出判断)如果现象为b为“产生气泡,固体部分溶解”,则猜想_____成立;
如果现象b为_____,则猜想_____成立。