题目内容
【题目】向盛有一定质量稀硫酸的烧杯中逐渐加入10g锌粒,产生气体质量与锌粒质量的关系如图所示;充分反应后,称得烧杯中剩余物质总质量为109.8g。请根据关系图分析并计算:
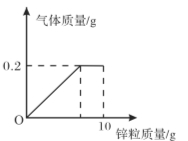
(1)稀硫酸反应完时,产生氢气的质量为 g,消耗锌粒质量为 g。
(2)该稀硫酸中溶质的质量分数(写出计算过程)。
【答案】(1)0.2 6.5 (2)9.8%。
【解析】
试题分析:根据图像可知,产生氢气的质量是0.2 g
解:设产生0.2 g氢气时参加反应的硫酸的质量为x,消耗锌的质量是y
Zn + H2SO4 = ZnSO4 + H2 ↑
65 98 2
y x 0.2g
![]()
![]() =
=![]()
解得 x =9.8g, y=6.5 g
根据质量守恒定律得稀硫酸的质量:109.8g+0.2g-10g=100g
∴稀硫酸中溶质的质量分数=![]() ×100%=9.8%
×100%=9.8%
答:产生氢气的质量是0.2 g,消耗锌的质量是6.5 g,该稀硫酸中溶质的质量分数为9.8%。

练习册系列答案
相关题目