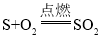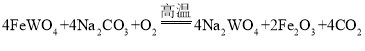题目内容
【题目】阅读资料并回答问题
钠(Na)是一种银白色金属,质软而轻,可用小刀切割,密度比水小,为 0.97g/cm3,熔点97.81℃,沸点 882.9℃。钠刚切开时,新切面有银白色光泽,但在空气中马上氧化转变为暗灰色。钠能与水发生剧烈反应生成氢氧化钠和氢气,量大时发生爆炸。钠还能在二氧化碳中燃烧,生成纯碱和一种气体氧化物。金属钠往往浸放于液体石蜡、矿物油和苯系物中密封保存。
(1)贮存金属钠时,用液体石蜡包裹的作用是______;
(2)金属钠在二氧化碳中燃烧的反应方程式是_______。铷(Rb)是一种银白色蜡状金属,化学性质与金属钠很相似,但比金属钠更活泼,遇水即在表面发生剧烈的反应并发生爆炸,该反应可表达为:
![]()
(3)推测溶液A中可能含有一种我们非常熱悉的离子____(填微粒符号),并设计3个不同的实验方案对此猜想进行验证。限选试剂:MgCl2溶液、CuSO4溶液、Na2CO3溶液、NaOH溶液、稀盐酸、酚酞溶液、紫色石蕊溶液、镁条、碳粉、氧化铁。
方案 | 验证预测的实验操作 | 预期现象 |
1 | 取少量溶液A于试管中,滴入____,振荡观察。 | 如果观察到___________则预测成立。 |
2 | 取少量溶液A于试管中,滴入____,振荡观察。 | 如果观察到___________则预测成立。 |
3 | 取少量溶液A于试管中,滴入_____,振荡观察。 | 如果观察到________________则预测成立。 |
【答案】隔绝金属钠与氧气(空气) 2Na +2CO2![]() Na2CO3+CO OH- 酚酞溶液/石蕊溶液 无色酚酞变红/紫色石蕊变蓝 MgCl2溶液 产生白色沉淀 CuSO4溶液 产生蓝色沉淀
Na2CO3+CO OH- 酚酞溶液/石蕊溶液 无色酚酞变红/紫色石蕊变蓝 MgCl2溶液 产生白色沉淀 CuSO4溶液 产生蓝色沉淀
【解析】
(1)根据资料,钠刚切开时,新切面有银白色光泽,但在空气中马上氧化转变为暗灰色。说明金属钠很容易跟氧气反应,所以贮存金属钠时,用液体石蜡包裹的作用是隔绝金属钠与氧气接触;
(2) 因为钠在二氧化碳中燃烧,生成纯碱和一种气体氧化物,所以金属钠在二氧化碳中燃烧的反应方程式是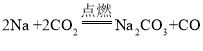 ;
;
⑶钠能与水发生剧烈反应生成氢氧化钠和氢气,铷【Rb】化学性质与金属钠很相似,根据![]() ,可见无色溶液A中含有OH-;为了验证OH-的存在,可以设计方案1.加入酚酞溶液/石蕊溶液如果出现酚酞溶液变红/石蕊溶液变蓝,则说明溶液中含OH-,猜想正确;方案2,加入MgCl2溶液,因为MgCl2+2NaOH=Mg(OH)2↓+2NaCl,所以如果出现白色沉淀,则溶液中一定含OH-,猜想正确;方案3,取少量溶液A于试管中,滴入CuSO4溶液,振荡观察,因为CuSO4+2NaOH=Cu(OH)2↓+Na2SO4,所以如果出现蓝色沉淀,则说明溶液中含OH-,猜想正确。
,可见无色溶液A中含有OH-;为了验证OH-的存在,可以设计方案1.加入酚酞溶液/石蕊溶液如果出现酚酞溶液变红/石蕊溶液变蓝,则说明溶液中含OH-,猜想正确;方案2,加入MgCl2溶液,因为MgCl2+2NaOH=Mg(OH)2↓+2NaCl,所以如果出现白色沉淀,则溶液中一定含OH-,猜想正确;方案3,取少量溶液A于试管中,滴入CuSO4溶液,振荡观察,因为CuSO4+2NaOH=Cu(OH)2↓+Na2SO4,所以如果出现蓝色沉淀,则说明溶液中含OH-,猜想正确。

 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案【题目】实验室有一瓶标签残缺并且瓶盖没有完全密封的无色溶液(如图),化学小组的同学经过询问老师后知道是NaCl、NaOH、Na2CO3、NaHCO3中的一种溶液,为确认原瓶中是何种溶质并判断是否变质,化学小组的同学进行了如下的探究活动:
(进行猜想)
猜想Ⅰ:原溶液的溶质是NaCl;
猜想Ⅱ:原溶液的溶质是NaOH;
猜想Ⅲ:原溶液的溶质是Na2CO3;
猜想Ⅳ:原溶液的溶质是NaHCO3。
(查阅资料)常温下,有关物质的相关信息如表:
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
常温下稀溶液的pH | 7 | 13 | 11 | 9 |
从物质的相关信息可知,原溶液的溶质一定不是NaHCO3,因为①_____。
(进行实验)
(1)取少量样品,测得溶液的pH大于7,则原溶液的溶质肯定不是②_____。
(2)同学们另取样品又进行了入如下实验,实验过程如下:
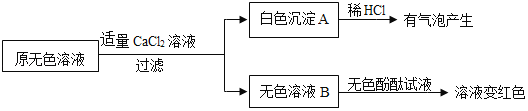
①生成白色沉淀A的化学方程式 ③_____。
②通过实验可以判断样品无色溶液中含有的溶质有 ④_____。
(获得结论)实验完成后,经过同学们讨论,最终得到的结论:原瓶中的溶质是 ⑤_____,且已变质。
(拓展应用)要除去部分变质的氢氧化钠溶液中的杂质,可选择适量的 ⑥_____ (填序号)。
A Ba(OH)2 溶液 B BaCl2溶液 C Ca(OH)2 溶液