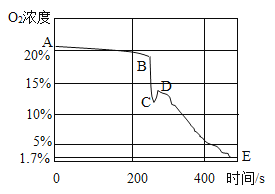
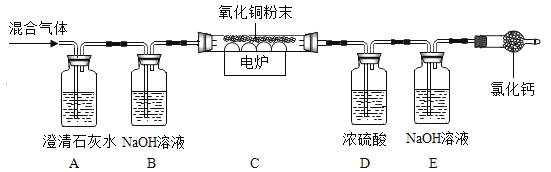
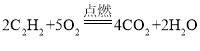��Ŀ����
����Ŀ��ij�����ų��ķ�ˮ�к���AgNO3��Ba( NO3)2 ��Cu(NO3)2�������ʡ�ij��ѧ��ȤС�����������ϣ����������ʵ�鷽��������ˮ��
[��������]
�ٰ�ɫ��Fe(OH)2�����ڳ�ʪ������Ѹ��ת��Ϊ���ɫFe( OH)3;
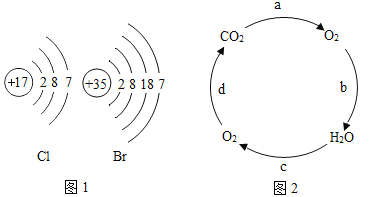
��Ba�Ľ�����Ա�Feǿ��
�����÷�ˮ��ʵ�鷽��.��������:
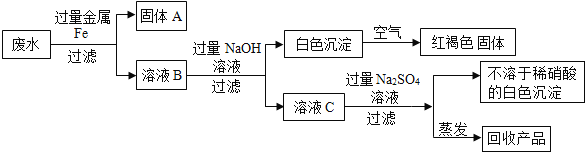
�ش���������:
(1)���ղ�Ʒ�к�������һ��������_________________����д��ѧʽ��
(2)д����ɫ�����ڿ�����ת��Ϊ���ɫ����Ļ�ѧ����ʽΪ______________________��
(3)�ڷ�ˮ����������Ҫ��������Լ���Ŀ����______________________��
(4)���������漰_________________�ֻ�����Ӧ���͡�
���𰸡�NaNO3 ![]() ȫ��ȥ������(��ʹ��Ҫ��ȥ������ȫ��Ӧ) 3
ȫ��ȥ������(��ʹ��Ҫ��ȥ������ȫ��Ӧ) 3
��������
��ˮ�м�����������ۣ������A��Ϊ�����������Լ��û�����������ͭ����ҺB�к����������������ᱵ���������������������Һ���ˣ���ɫ������������������Ȼ���ڿ��������ɺ���ɫ����������������ҺC�к��������ơ����ᱵ�Լ��������������ƣ���������������ƣ��������ᱵ��ɫ���������������ᣬ�����ᾧ�õ������ƺ������������ƺ������ơ�
(1)���ղ�Ʒ�к��д����������ƺ������������ƣ��Լ������ƣ��������ƺ�����������Ӧ�����ᱵ�������Ʒ�Ӧ�������������ɣ���������һ�������ǣ�NaNO3��
(2) ��ɫ��Fe(OH)2�����ڳ�ʪ������������ˮ����Ѹ��ת��Ϊ���ɫFe( OH)3�Ļ�ѧ����ʽΪ![]() ��
��
(3)�ڷ�ˮ����������Ҫ��������Լ���Ŀ���ǣ�ʹ��Ҫ��ȥ������ȫ��Ӧ��
(4)�������У���������������Ӧ�����������������������û���Ӧ����������������������ˮ��Ӧ�����������������ڻ��Ϸ�Ӧ���������������������Ʒ�Ӧ�����ᱵ��Һ����������Һ��Ӧ�������ڸ��ֽⷴӦ�����漰3�ֻ�����Ӧ���͡�