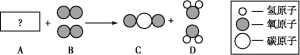
题目内容
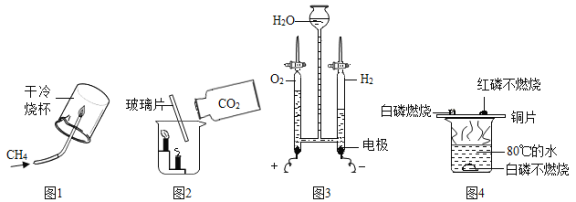
【题目】请结合图1回答问题:
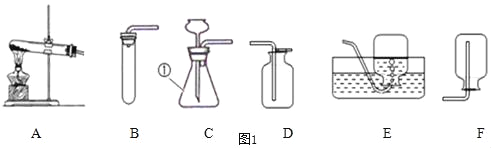
(1)写出标有①的仪器名称__________。
(2)实验室用高锰酸钾制取一瓶氧气,应选择上述装置中的A和_____(填装置序号)进行组装,而小明认为A装置中还缺少_____。该反应的化学方程式为______________。
(3)可用_____(填装置序号)收集CO2,检验CO2已收集满的方法是________________。
(4)①甲、乙、丙是同学们设计的一组“吹气球”的实验装置。
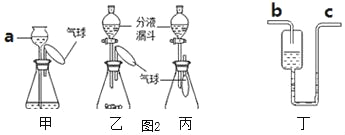
甲装置中,向a中加入一定量水后会看到气球胀大,一段时间内观察到______________,说明该装置气密性良好。
乙装置中,锥形瓶中装有氢氧化钠固体,从分液漏斗里向锥形瓶中加入适量水,气球胀大,其主要原因是______________。
丙装置中,锥形瓶中盛满CO2.从体积相同的少量下列物质中选择_____(填序号)加入,可使气球膨胀最大。
A.稀硫酸 B.氢氧化钠浓溶液 C.石灰水 D.水
②装置丁是同学们利用医用输液观察滴液快慢的滴壶,用它作微型洗气装置,气体应从_____(填“b”或“c”)进入,其中洗气的液体不能装满的原因是______________。
【答案】锥形瓶;D(或E);棉花;2KMnO4![]() K2MnO4+MnO2+O2↑;D;将燃着的木条放在集气瓶口,若燃着的木条熄灭,则二氧化碳已收集满;长颈漏斗中的液面高度不变(或气球大小不变)(其他合理答案也可);NaOH溶于水放热;B;c;装满了不利于气体从b中导出(或其他合理答案)。
K2MnO4+MnO2+O2↑;D;将燃着的木条放在集气瓶口,若燃着的木条熄灭,则二氧化碳已收集满;长颈漏斗中的液面高度不变(或气球大小不变)(其他合理答案也可);NaOH溶于水放热;B;c;装满了不利于气体从b中导出(或其他合理答案)。
【解析】
(1)仪器①是锥形瓶。
(2)氧气的密度比空气大,不易溶于水,所以可用向上排空气法D来收集,或排水法E来收集;为了防止高锰酸钾颗粒进入导气管,需要在试管口放置一团棉花;高锰酸钾在加热的条件下分解为锰酸钾、二氧化锰和氧气,反应方程式为2KMnO4![]() K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
(3)二氧化碳溶于水,不能采用排水法收集,密度比空气大,可以采用向上排空气法D收集,二氧化碳密度比空气大,二氧化碳不会燃烧,也不支持燃烧,所以验满时可将燃着的木条放在集气瓶口,观察木条是否熄灭。
(4)①甲装置中,向a中加入一定量水后会看到气球胀大,一段时间内观察到长颈漏斗中的液面高度不变或气球大小不变,说明该装置气密性良好。
氢氧化钠固体溶于水后会放出热量,造成装置内的气体受热膨胀,压强变大,所以观察到气球胀大;
稀硫酸与二氧化碳不反应,二氧化碳能与氢氧化钠、氢氧化钙和水反应,而其中氢氧化钠浓溶液(体积相同)吸收的二氧化碳最多,所以气球膨胀最大,故选B;
②医用输液观察滴夜快慢的滴壶,若用它作微型洗气装置,则气体应从c进入,其中所装洗气的液体不能装满的原因是通入的气体可能会把洗气液体压出滴壶。

【题目】金属与人类的生产、生活密切相关,牢固掌握金属的知识十分必要。
(1)下列用途是利用了金属的导电性的是________(填字母代号)。
A.铜作导线 B.金作戒指
C.铝合金作门窗 D.铁锅作炊具
(2)将一小块金属钠放入滴有无色酚酞溶液的水中,钠剧烈反应,可观察到其熔成小球,在水面上游动,溶液变成红色。
①请根据上述现象总结金属钠的物理性质(写出两点即可)_________________。
②已知该反应还产生了一种可燃性气体,请写出此反应的化学方程式_______________。
(3)将锌粉加到含有 Cu(NO3)2 和 AgNO3 的混合溶液中,充分反应后过滤。
①若滤液中只含有一种溶质,请分析滤渣的成分_______________。
②若滤渣中含有两种金属,请分析滤液的成分_______________。
(4)合金的种类很多,用途十分广泛,黄铜是铜和锌的合金,它可以用来制造机器和电器的零件等,化学兴趣小组的同学欲测定某铜样品中铜的质量分数(不考虑黄铜中的其他杂质),请你参与他们的探究过程。称量 10 g 粉末状黄铜样品放入烧杯中,量取 45 mL 稀盐酸分三次加入其中,每次充分反应后,测定生成氢气的质量,实验数据如表:
第一次 | 第二次 | 第三次 | |
加入稀盐酸的体积(mL) | 15 | 15 | 15 |
生成氢气的质量(g) | 0.04 | m | 0.02 |
试计算:①m 的数值为________。
②此黄铜样品中铜的质量分数是多少__________________