题目内容
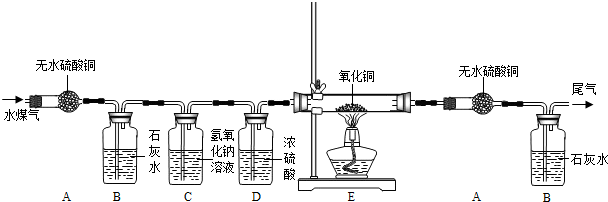
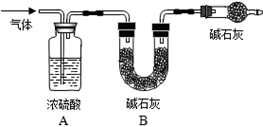
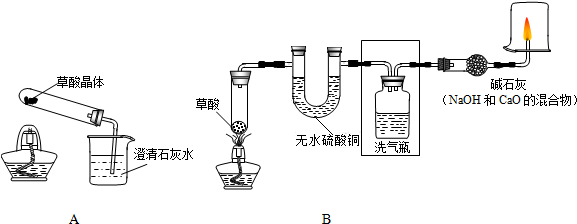
过氧化钠(Na2O2)是一种淡黄色粉末,可作为潜水艇或呼吸面具有供氧剂.人呼出气体的主要成分有氮氧、氧气、二氧化碳和水蒸气,二氧化碳和水能分别与Na2O2反应生成氧气.为了探究Na2O2在潜水艇中反应后的物质,明明同学设计了如图1所示模拟实验.

【猜想与假设】
(1)明明猜想生成的固体物质是:(Ⅰ)氢氧化钠(Ⅱ)碳酸钠(Ⅲ)氢氧化钠和碳酸钠.
【实验与验证】
明明通过以下实验探究来验证他的猜想:
①取少量反应后干燥管中的固体样品,置于试管中,向其中加入______,发现有气泡产生,该气体通入澄清石灰水,石灰水变浑浊,证明猜想(Ⅰ)不成立.
②已知碳酸钠的水溶液呈碱性.请根据部分物质的溶解性表(20℃)所提供的信息,将明明的探究过程填写完整.
于是明明得出结论:猜想(Ⅱ)不成立,猜想(Ⅲ)成立.
【反思与评价】
(2)你认为Na2O2与______填(“二氧化碳”或“水”)反应生成了碳酸钠.在上述实验装置中再增加一个装置,重复步骤①即可证明你的判断,请指出应增加装置的名称和位置.
【拓展与延伸】
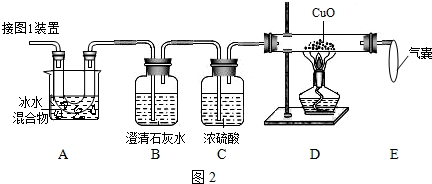
(3)另取少量反应后干燥管中的固体样品,配制成溶液,向其中逐滴滴加稀盐酸,产生气体的质量与加入稀盐酸的质量的关系如图2所示.
①请解释开始滴加盐酸时没有产生气体的原因.
②计算该样品中碳酸钠的质量.

【猜想与假设】
(1)明明猜想生成的固体物质是:(Ⅰ)氢氧化钠(Ⅱ)碳酸钠(Ⅲ)氢氧化钠和碳酸钠.
【实验与验证】
明明通过以下实验探究来验证他的猜想:
①取少量反应后干燥管中的固体样品,置于试管中,向其中加入______,发现有气泡产生,该气体通入澄清石灰水,石灰水变浑浊,证明猜想(Ⅰ)不成立.
②已知碳酸钠的水溶液呈碱性.请根据部分物质的溶解性表(20℃)所提供的信息,将明明的探究过程填写完整.
| 实验目的 | 实验操作 | 现象或测定结果 | 结论或化学方程式 |
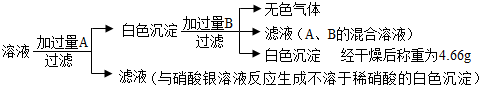
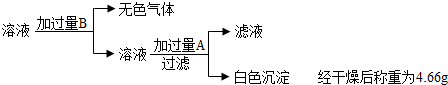
| 除去碳酸钠 | 取少量该固体样品溶于水配成溶液,滴加适量的______溶液,充分反应后过滤 | 有白色沉淀生成 | 有关反应的化学方程式为______ |
| 检验是否含有氢氧化钠 | 用PH试纸测定反应后溶液的酸碱度,操作方法是______ | pH>7 | 该样品中含有氢氧化钠 |
【反思与评价】
(2)你认为Na2O2与______填(“二氧化碳”或“水”)反应生成了碳酸钠.在上述实验装置中再增加一个装置,重复步骤①即可证明你的判断,请指出应增加装置的名称和位置.
【拓展与延伸】
(3)另取少量反应后干燥管中的固体样品,配制成溶液,向其中逐滴滴加稀盐酸,产生气体的质量与加入稀盐酸的质量的关系如图2所示.
①请解释开始滴加盐酸时没有产生气体的原因.
②计算该样品中碳酸钠的质量.
(1)①过氧化钠(Na2O2)二氧化碳反应生成了碳酸钠,碳酸钠能与稀盐酸反应生成二氧化碳;
②碳酸钠能与含钙离子的氯化钙溶液反应生成碳酸钙沉淀解答;反应的化学方程式为:Na2CO3+CaCl2═CaCO3↓+2NaCl;
用PH试纸测定反应后溶液的酸碱度,操作方法是:用玻璃棒蘸取溶液滴到pH试纸上,把试纸显示的颜色与标准比色卡比较.
(2)要证明Na2O2与二氧化碳反应生碳酸钠,需把人体呼出的水蒸气除去,因为过氧化钠也能与水反应生成氢氧化钠和氧气,故需在A、B之间增加一个盛装浓硫酸的干燥装置.
(3)①干燥管中的固体是氢氧化钠和碳酸钠的混合物,有氢氧化钠滴加盐酸时不会产生二氧化碳气体;
②设参加反应的碳酸钠的质量为x.
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
x 0.44 g
=
x=1.06 g
答,样品中碳酸钠的质量1.06 g.
答案:(1)①稀盐酸
②CaCl2;Na2CO3+CaCl2═CaCO3?+2NaCl;用玻璃棒蘸取溶液滴到pH试纸上,把试纸显示的颜色与标准比色卡比较.
(2)二氧化碳;在A、B之间增加一个盛装浓硫酸的干燥装置.
(3)①盐酸与氢氧化钠发生了反应,
②1.06 g.
②碳酸钠能与含钙离子的氯化钙溶液反应生成碳酸钙沉淀解答;反应的化学方程式为:Na2CO3+CaCl2═CaCO3↓+2NaCl;
用PH试纸测定反应后溶液的酸碱度,操作方法是:用玻璃棒蘸取溶液滴到pH试纸上,把试纸显示的颜色与标准比色卡比较.
(2)要证明Na2O2与二氧化碳反应生碳酸钠,需把人体呼出的水蒸气除去,因为过氧化钠也能与水反应生成氢氧化钠和氧气,故需在A、B之间增加一个盛装浓硫酸的干燥装置.
(3)①干燥管中的固体是氢氧化钠和碳酸钠的混合物,有氢氧化钠滴加盐酸时不会产生二氧化碳气体;
②设参加反应的碳酸钠的质量为x.
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
x 0.44 g
| 106 |
| 44 |
| 32 |
| 0.44g |
x=1.06 g
答,样品中碳酸钠的质量1.06 g.
答案:(1)①稀盐酸
②CaCl2;Na2CO3+CaCl2═CaCO3?+2NaCl;用玻璃棒蘸取溶液滴到pH试纸上,把试纸显示的颜色与标准比色卡比较.
(2)二氧化碳;在A、B之间增加一个盛装浓硫酸的干燥装置.
(3)①盐酸与氢氧化钠发生了反应,
②1.06 g.

练习册系列答案
相关题目