题目内容
【题目】根据下图回答问题。
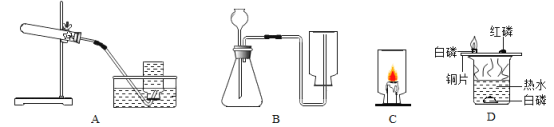
(1)实验室用装置A制取氧气,反应的化学方程式是_____,用排水集气法收集氧气,如何知道已收集满_____。
(2)实验室用B装置制取二氧化碳,装置中要改正的是_____,燃着的木条放在集气瓶口,若观察到_____,说明集气瓶中已充满二氧化碳。
(3)将上述实验收集的一瓶气体倒扣在燃着的蜡烛上(如图C所示),观察到蜡烛火焰更加明亮,一段时间后逐渐熄灭,则集气瓶中原有的气体是_____。
(4)D为探究燃烧条件的实验,其中热水作用是_____。
【答案】![]() 集气瓶口有气泡冒出 集气瓶口正放 火焰熄灭 O2 隔绝氧气;给铜片加热,使铜片上的白磷温度达到着火点
集气瓶口有气泡冒出 集气瓶口正放 火焰熄灭 O2 隔绝氧气;给铜片加热,使铜片上的白磷温度达到着火点
【解析】
(1)实验室用高锰酸钾法制取氧气用装置A,反应原理是高锰酸钾在加热条件下分解生成锰酸钾、二氧化锰、氧气,化学方程式是![]() ,用排水集气法收集氧气,集气瓶口有气泡冒出,说明已收集满氧气;
,用排水集气法收集氧气,集气瓶口有气泡冒出,说明已收集满氧气;
(2)实验室用B装置制取二氧化碳,装置中要改正的是集气瓶口应向上放置(正放),因二氧化碳的密度比空气的大且能溶于水,只能用向上排空气法收集;二氧化碳不可燃、不助燃,能使燃着的木条熄灭,故将燃着的木条放在集气瓶口,若观察到火焰熄灭,说明集气瓶中已充满二氧化碳;
(3)将上述实验收集的一瓶气体倒扣在燃着的蜡烛上(如图C所示),观察到蜡烛火焰更加明亮,一段时间后逐渐熄灭,则集气瓶中原有的气体是氧气,因氧气有助燃性,所以开始蜡烛燃烧更旺,后因烧杯内氧气耗尽,蜡烛熄灭;
(4)D为探究燃烧条件的实验,其中热水作用是:隔绝氧气;给铜片加热,使铜片上的白磷温度达到着火点。

 一本好题口算题卡系列答案
一本好题口算题卡系列答案【题目】长久使用热水壶底部有层水垢,主要成分为CaCO3和Mg(OH)2,某学校化学研究小组的同学通过实验测定水垢中CaCO3的含量:将过量的稀盐酸加入到200g水垢中,把产生的CO2气体用足量的NaOH溶液吸收,同时测量3min钟内NaOH溶液增加的质量,结果如下表:
时间/s | 0 | 30 | 60 | 90 | 120 | 150 | 180 |
质量/g | 0 | 30 | 50 | 60 | 66 | 66 | 66 |
(1)写出CO2被足量的NaOH溶液吸收时,发生的化学反应方程式_______________。
(2)从表格中可以看出,200g水垢与盐酸反应生成的CO2最多是___________g。
(3)计算水垢中碳酸钙的质量分数,写出计算过程_________