题目内容
(1)向盛有一定量氢氧化钠溶液(滴加有酚酞)的烧杯中加入盐酸,要控制盐酸的用量,其操作方法是:________;能够说明盐酸和氢氧化钠溶液恰好完全中和的实验现象是________.
(2)现实验室有失落标签的3瓶无色溶液:NaCl、HCl、NaOH,请设计一个实验方案,把这3瓶无色溶液区分开来.叙述实验操作、预期现象和结论.(实验室仅提供酚酞试液、蒸馏水以及常用的实验仪器)
| 实验步骤 | 预期现象与结论 |
| ①________ | ________ |
| ②________ | ________ |
解:(1)酚酞试液遇到碱溶液变红色,酸与碱中和时红色消失,其操作方法是:向烧杯中滴加盐酸,边滴加边振荡;当滴入最后一滴盐酸时,红色恰好消失,证明恰好中和.故答案为:向烧杯中滴加盐酸,边滴加边振荡;当滴入最后一滴盐酸时,红色恰好消失;
(2)题目给出的药品是:酸、碱和显中性的氯化钠,本题是用了无色的酚酞试液,因此就需要两个步骤,第一步先鉴别出碱,然后再利用酸和碱发生中和反应,依次鉴别出酸和盐.故答案为:①取三种溶液少许放入三支试管中,分别滴加酚酞试液;变红色的是氢氧化钠溶液,其它两种无变化;②在两种无变化的溶液中,任取一种去滴加试管中变红色的溶液;如果红色消失,那么滴加的是盐酸,剩余的是氯化钠溶液.
分析:本题属于鉴别题,题目给出的药品是:酸、碱和显中性的盐.如果用石蕊试液就可以一次鉴别;本题是用了无色的酚酞试液,因此就需要两个步骤,第一步先鉴别出碱,然后再利用酸和碱发生中和反应,依次鉴别出酸和盐.酚酞试液遇到碱溶液变红色,酸与碱中和时红色消失,其操作方法是:向烧杯中滴加盐酸,边滴加边振荡;当滴入最后一滴盐酸时,红色恰好消失,证明恰好中和.
点评:本考点属于常见离子的检验方法,如氢离子、氢氧根离子、氯离子、硫酸根离子、铵根离子等的检验方法是中考的重要考点,要根据它们的性质选择所用的试剂,然后由现象得出结论.本考点经常出现在选择题、填空题和实验题中.
(2)题目给出的药品是:酸、碱和显中性的氯化钠,本题是用了无色的酚酞试液,因此就需要两个步骤,第一步先鉴别出碱,然后再利用酸和碱发生中和反应,依次鉴别出酸和盐.故答案为:①取三种溶液少许放入三支试管中,分别滴加酚酞试液;变红色的是氢氧化钠溶液,其它两种无变化;②在两种无变化的溶液中,任取一种去滴加试管中变红色的溶液;如果红色消失,那么滴加的是盐酸,剩余的是氯化钠溶液.
分析:本题属于鉴别题,题目给出的药品是:酸、碱和显中性的盐.如果用石蕊试液就可以一次鉴别;本题是用了无色的酚酞试液,因此就需要两个步骤,第一步先鉴别出碱,然后再利用酸和碱发生中和反应,依次鉴别出酸和盐.酚酞试液遇到碱溶液变红色,酸与碱中和时红色消失,其操作方法是:向烧杯中滴加盐酸,边滴加边振荡;当滴入最后一滴盐酸时,红色恰好消失,证明恰好中和.
点评:本考点属于常见离子的检验方法,如氢离子、氢氧根离子、氯离子、硫酸根离子、铵根离子等的检验方法是中考的重要考点,要根据它们的性质选择所用的试剂,然后由现象得出结论.本考点经常出现在选择题、填空题和实验题中.

练习册系列答案
相关题目
我们在学习碳酸钠和碳酸氢钠的时候,做过如图装置的实验.
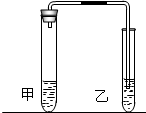
向盛有0.5g碳酸钠的试管里加入2mL盐酸,迅速用带导管的胶塞塞紧试管口,并将导管另一端通入盛有澄清石灰水的试管中,观察现象.
用碳酸氢钠代替碳酸钠进行上述实验,观察现象.
(1)通过比较试管甲中的两次反应,填写下表:
写出乙中反应的化学方程式: .
(2)某同学对碳酸钠和碳酸氢钠与盐酸反应的快慢进一步研究.在老师的指导下,设计了下面的实验探究方案.
实验用品:相同型号的U型管2支、橡皮塞2个、5mL一次性注射器2支、气球个.
实验装置:如图.
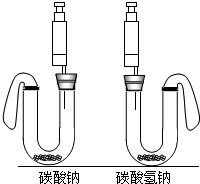
实验操作:在U型管中分别加入一定量碳酸钠和碳酸氢钠固体,在两支注射器中分别吸入同溶质质量分数、同体积的足量稀盐酸.将注射器插入橡皮塞中,然后同时迅速将盐酸分别注入U型管中.请对上述实验方案分析评价.
①若取用碳酸钠0.53g,为控制实验中产生气体的量相同,应取用碳酸氢钠 g;
②该同学设计的实验方案是运用了 研究的方法;
③实验过程中需要观察的现象是 .

向盛有0.5g碳酸钠的试管里加入2mL盐酸,迅速用带导管的胶塞塞紧试管口,并将导管另一端通入盛有澄清石灰水的试管中,观察现象.
用碳酸氢钠代替碳酸钠进行上述实验,观察现象.
(1)通过比较试管甲中的两次反应,填写下表:
| 碳酸钠+盐酸 | 碳酸氢钠+盐酸 | |
| 实验现象 | 反应迅速,生成大量气体. | 反应 |
| 实验结论 | ||
(2)某同学对碳酸钠和碳酸氢钠与盐酸反应的快慢进一步研究.在老师的指导下,设计了下面的实验探究方案.
实验用品:相同型号的U型管2支、橡皮塞2个、5mL一次性注射器2支、气球个.
实验装置:如图.

实验操作:在U型管中分别加入一定量碳酸钠和碳酸氢钠固体,在两支注射器中分别吸入同溶质质量分数、同体积的足量稀盐酸.将注射器插入橡皮塞中,然后同时迅速将盐酸分别注入U型管中.请对上述实验方案分析评价.
①若取用碳酸钠0.53g,为控制实验中产生气体的量相同,应取用碳酸氢钠
②该同学设计的实验方案是运用了
③实验过程中需要观察的现象是
长期露置在空气中的铜器表面有一层绿色固体.小强带着浓厚的兴趣对该绿色固体的元素组成进行研究.请你结合下列装置图回答问题.

查阅资料:金属铜长时间放置在空气中,与氧气等物质发生复杂的化学反应,形成“铜绿”.
空气中氮气和稀有气体的化学性质稳定,常温下难与其他物质反应.
猜想与假设:经过思考和推理,小强认为“铜绿”的组成元素可能是铜、氧、氢、碳元素.
实验与结论:小强按实验设计连接A→______→______装置(填装置代号),在检查装置气密性后进行相关实验.请你帮助小强完成下列实验报告:
小李和小王两位同学对碱式碳酸铜[Cu2(OH)2CO3]受热完全分解后的黑色固体的成分进行探究.
(1)小李根据碱式碳酸铜的化学式对黑色固体产物做出以下猜想:①可能是碳,②可能是氧化铜.③可能是碳和氧化铜的混合物.他做出以上猜想的依据是______;
(2)小王根据碳的化学性质,认为猜想③可以排除,理由是______;
(3)为验证①、②猜想,他们设计如下实验方案:向盛有少量黑色固体的试管中加入足量的稀硫酸,振荡,待完全反应后静置观察现象.若猜想①正确,现象应该是______;若猜想②正确,现象应该是______.
通过实验探究得知“铜绿”是由铜、氧、氢、碳四种元素组成.
反思与应用:大多数金属的锈蚀与铁、铜的锈蚀相似,金属的锈蚀给人类带来了巨大的损失,请写出防止金属锈蚀的一种方法:______.

查阅资料:金属铜长时间放置在空气中,与氧气等物质发生复杂的化学反应,形成“铜绿”.
空气中氮气和稀有气体的化学性质稳定,常温下难与其他物质反应.
猜想与假设:经过思考和推理,小强认为“铜绿”的组成元素可能是铜、氧、氢、碳元素.
实验与结论:小强按实验设计连接A→______→______装置(填装置代号),在检查装置气密性后进行相关实验.请你帮助小强完成下列实验报告:
| 实验操作 | 实验现象 | 实验结论 |
| 实验Ⅰ:将一定量绿色固体装入反应容器中,进行实验 | ①白色无水硫酸铜变蓝色 | 产物中有______ |
| ②______ | 产物中有二氧化碳 写出检验二氧化碳的化学方程式: ______ | |
| ③绿色固体变黑色 |
(1)小李根据碱式碳酸铜的化学式对黑色固体产物做出以下猜想:①可能是碳,②可能是氧化铜.③可能是碳和氧化铜的混合物.他做出以上猜想的依据是______;
(2)小王根据碳的化学性质,认为猜想③可以排除,理由是______;
(3)为验证①、②猜想,他们设计如下实验方案:向盛有少量黑色固体的试管中加入足量的稀硫酸,振荡,待完全反应后静置观察现象.若猜想①正确,现象应该是______;若猜想②正确,现象应该是______.
通过实验探究得知“铜绿”是由铜、氧、氢、碳四种元素组成.
反思与应用:大多数金属的锈蚀与铁、铜的锈蚀相似,金属的锈蚀给人类带来了巨大的损失,请写出防止金属锈蚀的一种方法:______.

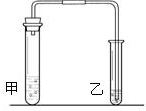 我们在学习碳酸钠和碳酸氢钠的时候,做过如下图装置的实验.向盛有0.5g碳酸钠的试管里加入2mL盐酸,迅速用带导管的胶塞塞紧试管口,并将导管另一端通入盛有澄清石灰水的试管中,观察现象.用碳酸氢钠代替碳酸钠进行上述实验,观察现象.
我们在学习碳酸钠和碳酸氢钠的时候,做过如下图装置的实验.向盛有0.5g碳酸钠的试管里加入2mL盐酸,迅速用带导管的胶塞塞紧试管口,并将导管另一端通入盛有澄清石灰水的试管中,观察现象.用碳酸氢钠代替碳酸钠进行上述实验,观察现象.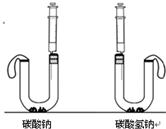 请对上述实验方案分析评价.
请对上述实验方案分析评价. (2012?香坊区二模)如图所示的烧杯中盛有一定量的稀硫酸,溶液中漂浮一个塑料块.请回答:
(2012?香坊区二模)如图所示的烧杯中盛有一定量的稀硫酸,溶液中漂浮一个塑料块.请回答: