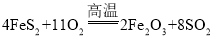题目内容
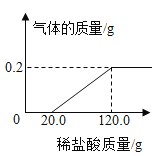
【题目】向盛有11.4gNa2CO3和Na2SO4的固体混合物的烧杯中,缓慢加入溶质质量分数为10%的稀硫酸,放出气体的总质量与所加入稀硫酸的质量关系如图10所示。请计算:
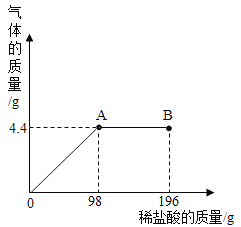
(1)生成二氧化碳的总质量为 。
(2)配制200g质量分数为10%的稀硫酸,需质量分数98%的浓硫酸 g。
(3)当加入稀硫酸至图中A点时,溶液中溶质的质量分数(烧杯中为不饱和溶液)。
【答案】(1)4.4g;(2)20.4;(3)14.3%
【解析】
碳酸钠与硫酸反应生成硫酸钠、水和二氧化碳,硫酸钠不与硫酸反应。
(1)由图可知,生成二氧化碳的质量为4.4g;
(2)200g质量分数为10%的稀硫酸中溶质质量为:200g×10%=20g;需质量分数98%的浓硫酸的质量为:20g÷98%≈20.4g;
(3)设固体混合物中碳酸钠的质量为x,生成硫酸钠的质量为y
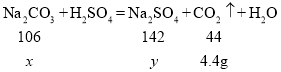
![]() x=10.6g
x=10.6g
![]() y=14.2g
y=14.2g
当加入稀硫酸至图中A点时,溶液中溶质的质量分数为:![]() 。
。
答:当加入稀硫酸至图中A点时,溶液中溶质的质量分数为14.3%。

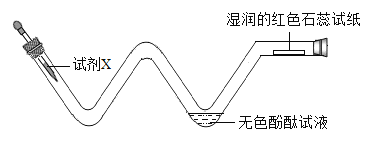
【题目】向一定量的NaOH溶液中慢慢通入CO2气体,看不到明显现象。某实验小组的同学对所得溶液成分进行了如下探究。请你参与他们的探究活动,并完成以下问题:
(提出问题)所得溶液中溶质的成分是什么?
(査阅资料)资料一:将CO2气体慢慢地通入一定量的NaOH溶液中,可能发生以下两个化学反应:
先发生反应:2NaOH+CO2═Na2CO3+H2O
当NaOH反应完全后,继续发生反应:Na2CO3+CO2+H2O═2NaHCO3
資料二;Ca(HCO3)2易溶于水;CaCl2溶液与NaCl溶液均呈中性; NaHCO3溶液呈碱性,可使酚酞溶液变红色。
(猜想与假设)小组同学通过讨论,提出了以下四种猜想
猜想一:溶质为NaOH和Na2CO3
猜想二:溶质全为Na2CO3
(1)你认为猜想三:溶质为_____
猜想四:溶质全为 NaHCO3
(实验探究)小组同学设计并完成了如下实验:
实验步骤 | 实验过程 | 实验现象 | 实验结论 |
① | 取适量反应后的溶液置于试管 中,加入过量CaCl2溶液 | 有白色沉淀生成 | (2)猜想_____不成立 |
② | 取适量步骤①反应后的上层清 液,滴加几滴酚酞溶液 | (3)现象为_____ | 猜想二不成立 |
③ | 取适量步骤①反应后的上层清 液,加入适量稀HCl | 有气泡产生 | (4)猜想_____成立 |
(实验总结)针对上述实验,实验小组的同学总结并写出了上述探究过程中的各步反应方程式。
(5)你认为步骤①发生反应的化学方程式是_____。
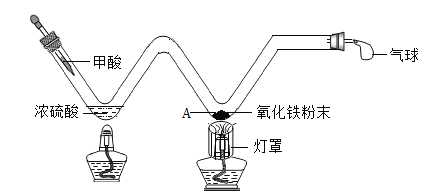
【题目】高阳同学通过阅读课外资料得知,潜水艇中常用过氧化钠(Na2O2)作为供氧剂,有关反应的化学方程式为:2Na2O2+2CO2═2Na2CO3+O2,2Na2O2+2H2O═4NaOH+O2↑。于是她用如图所的装置来制取CO2并验证其与Na2O2的反应。
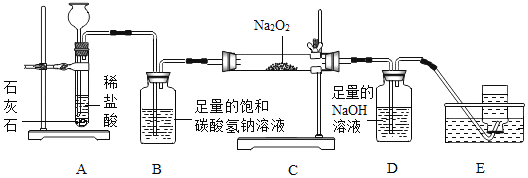
(1)装置B的作用是_____。
(2)反应一段时间后,装置E中收集到的气体主要是_____;反应后装置C硬质玻璃管中固体的成分是什么?高阳为此又进行了如下探究:
(猜想与假设)
猜想一 Na2CO3
猜想二Na2CO3和Na2O2
猜想三Na2CO3和NaOH
你认为还可能是_____
(设计实验)
实验操作 | 实验现象 | 实验结论 |
①取少量样品于试管中,加入足量的水,振荡 | 固体完全溶解,_____ | 样品中一定没有Na2O2 |
②取少量实验①所得溶液于另一试管中,加入过量的BaCl2溶液,振荡 | 有白色沉淀产生 | 猜想三正确 |
③取少量实验②所得上层清液于另一试管中,加入_____溶液,振荡 | 有白色沉淀产生 |
(反思与评价)反应后装置C硬质玻璃管中的固体含有NaOH,原因可能是_____。