题目内容
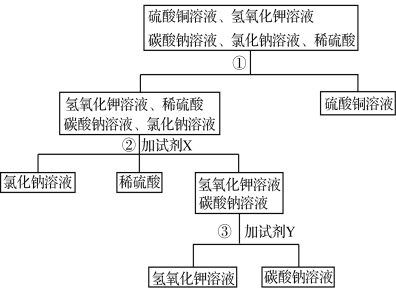
【题目】甲、乙两种固态物质的饱和溶液中溶质质量分数与温度关系如图所示。
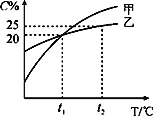
(1)甲、乙两种物质的溶解度随温度升高而_________(填“增大”或“减小”)。
(2)t1℃时,乙固体的溶解度为:________。
(3)25g乙物质完全溶于100g水所需的最低温度是_____。
(4)t2℃100g乙饱和溶液,稀释成10%乙溶液用到的玻璃仪器有_____________。
(5)根据图形分析,下列说法正确的是_____。
A t1℃甲、乙两种物质饱和溶液中溶质质量相等
B 将t1℃甲、乙饱和溶液升温至t2℃,所得溶液溶质质量分数相等
C t2℃,若从甲、乙两物质饱和溶液中析出等质量固体,蒸发较多水的是甲饱和溶液
D 甲中混有少量乙,提纯甲固体,可采用降温结晶的方法
【答案】增大 25g t1℃ 量筒、胶头滴管、烧杯、玻璃棒、 BD
【解析】
(1)通过分析图像可知,甲、乙两种物质的溶解度都随温度升高而增大。
(2)由图像可知,t1℃时,乙固态物质的饱和溶液中溶质质量分数为20%,设t1℃时,乙物质的溶解度为x,则![]() ×100% =20%,解得x=25g
×100% =20%,解得x=25g
(3)25g乙物质完全溶于100g水中,所得饱和溶液的溶质质量分数为:![]() ×100%=20%,乙饱和溶液中溶质质量分数为20%所对应的温度是t1℃。
×100%=20%,乙饱和溶液中溶质质量分数为20%所对应的温度是t1℃。
(4)将一定质量的浓溶液稀释为稀溶液,需要用到的玻璃仪器有量筒、胶头滴管、烧杯、玻璃棒。
(5)A.t1℃时,等质量的甲、乙两种物质饱和溶液中溶质质量相等,题中没有明确溶液质量,所以溶质质量不一定相等,此选项错误;B.由于t1℃甲、乙饱和溶液的溶质质量分数相等,将t1℃甲、乙饱和溶液升温至t2℃,溶解度变大,溶质质量分数不变,所得溶液溶质质量分数相等,此选项正确;C.由图像可知,t2℃时,甲的溶解度大于乙的溶解度,所以若从甲、乙两物质饱和溶液中析出等质量固体,蒸发较多水的是乙饱和溶液,此选项错误;
D.甲的溶解度受温度影响较大,所以提纯甲固体,可采用降温结晶的方法,此选项正确。故选BD。

 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案【题目】厨师在厨房炒菜时加了料后再加醋,就让菜肴变得香美可口,这其实隐藏了一个化学的小秘密:醋中的乙酸与料酒中的乙醇反应生成了有香味的乙酸乙酯,下表中是几种常见的酯,请完成下列问题:
酯的名称 | 甲酸甲酯 | 乙酸乙酯 | 丙酸丙酯 | 丁酸丁酯 |
化学式 | C2H4O2 | C4H8O2 | C6H12O2 | X |
(1)甲酸甲酯中碳元素、氢元素、氟元素的质量比为_____,其中氢元素的质量分数为_____;(保留0.1%)
(2)比较归纳是学习的重要方法,根据表推测X的化学式是_____;
(3)丙酸丙酯中氧元素的质量分数_____(填“大于”、“小于”或“等于”)丁酸丁酯中氧元素的质量分数;
(4)若菜肴中的乙酸乙酯在人体内代谢时其中的碳元素完全部转化为CO2,则44mg的乙酸乙酯完全代谢产生的CO2的质量为多少?(请写出计算过程)_________
【题目】小明设计实验探究“锌与硫酸反应快慢的影响因素”实验数据如表
实验编号 | 硫酸的质量分数 | 硫酸的体积/mL | 锌 | 锌的质量/g | 3分钟收集的氢气体积/mL |
① | 20% | 20 | 锌块 | 1 | 31.7 |
② | 20% | 20 | 锌箔 | 1 | 50.9 |
③ | 30% | 20 | 锌块 | 1 | 61.7 |
④ | 30% | 20 | 锌箔 | 1 | 79.9 |
(1)小明做此实验想要验证的假设是______;
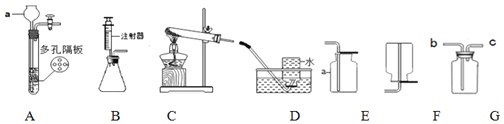
(2)小明用如图装置收集并测量氢气的体积,导管c应与______相连(填“a”或“b”)
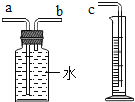
(3)如表是小明第①组实验的详细数据:
记录数据时间 | 第1分钟末 | 第2分钟末 | 第3分钟末 | 第4分钟末 | 第5分钟末 | 第6分钟末 |
量筒中水的体积/mL | 3.1 | 19.8 | 31.7 | 41.3 | 48.9 | 54.9 |
已知锌和硫酸反应是放热反应,请据如表数据描述锌与硫酸反应的速率变化情况,并作出合理解释______.
【题目】工业上用废铜料溶于加入氧化剂![]() 如
如![]() 的过氧化氢溶液
的过氧化氢溶液![]() 的稀硫酸得到大量高纯度的硫酸铜。反应过程中产生大量无色无味的气体,某兴趣小组对于该气体的成分进行了如下探究。
的稀硫酸得到大量高纯度的硫酸铜。反应过程中产生大量无色无味的气体,某兴趣小组对于该气体的成分进行了如下探究。
![]() 探究该气体的成分是什么?
探究该气体的成分是什么?
(假设与猜想)
小明认为不可能是二氧化硫,理由是:______;
![]() 小亮认为不可能是氢气,理由是:______;小红认为是氧气。
小亮认为不可能是氢气,理由是:______;小红认为是氧气。
![]() (实验探究)
(实验探究)
实验步骤 | 实验现象 | 实验结论 |
取少量铜屑于试管中,滴加 | 溶液由无色变为 ______ 色,带火星的木 ______ 。 | 该气体是 ______ 。 |
![]() 写出放出气体的反应的化学方程式:______。
写出放出气体的反应的化学方程式:______。
常温下过氧化氢分解缓慢,产生的氧气量很少,不足以使带火星的木条复燃。试通过实验验证是硫酸铜加快了过氧化氢的分解速率,请写出实验设计方案。
实验步骤 | 实验现象 | 实验结论 |
______ | ______ | ______ |