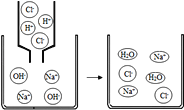
��Ŀ����
����Ŀ�����ǵ��ճ������ũҵ�����벻��ˮ����ش�����ˮ��������⡣
![]() �й�ˮ��ʵ��װ����ͼ��ʾ��
�й�ˮ��ʵ��װ����ͼ��ʾ��
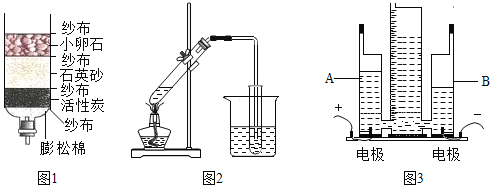
![]() ͼ1Ϊ����ˮװ�ã����л���̿��������______��
ͼ1Ϊ����ˮװ�ã����л���̿��������______��
![]() ͼ2Ϊ����װ�ã���ˮ�ֱ�ͼ2��ͼ1װ�õ�������������ˮ�ʳɷֵ�������______
ͼ2Ϊ����װ�ã���ˮ�ֱ�ͼ2��ͼ1װ�õ�������������ˮ�ʳɷֵ�������______
![]() ������ͼ1����õ�ˮ�Ƿ�ΪӲˮ�����õ��Լ���______
������ͼ1����õ�ˮ�Ƿ�ΪӲˮ�����õ��Լ���______
![]() ͼ3Ϊ����ˮ����������ˮ�Ĺ����е���ת��Ϊ______�ܡ�
ͼ3Ϊ����ˮ����������ˮ�Ĺ����е���ת��Ϊ______�ܡ�
![]() ͨ��һ��ʱ���A�Թ��в�����������______����______����A���е����塣
ͨ��һ��ʱ���A�Թ��в�����������______����______����A���е����塣
![]() ��B�������ɵ�����ۼ����ϲ���ԭ����______����A�����ռ�2L�����壬��B�����ռ����������ԼΪ______L
��B�������ɵ�����ۼ����ϲ���ԭ����______����A�����ռ�2L�����壬��B�����ռ����������ԼΪ______L
![]() ��ͼΪˮ��ͨ�������·ֽ���۹��̣�
��ͼΪˮ��ͨ�������·ֽ���۹��̣�
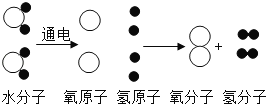
![]() ˮ�ķֽ�����У��������ı������______��
ˮ�ķֽ�����У��������ı������______��
![]() ���ʵ��������۵�ģ�ͱ仯������д����ѧʽ����ʽ______��
���ʵ��������۵�ģ�ͱ仯������д����ѧʽ����ʽ______��
![]() ���۵ĽǶȽ���ͼ2��ͼ3�еķ����仯�ı��ʲ�ͬ��______��
���۵ĽǶȽ���ͼ2��ͼ3�еķ����仯�ı��ʲ�ͬ��______��
![]() ��֪ͬ��ͬѹ�£�����������ȡ��������ķ��Ӹ����ȡ���ʵ�����ܹ�˵��ˮ�Ļ�ѧʽΪ��
��֪ͬ��ͬѹ�£�����������ȡ��������ķ��Ӹ����ȡ���ʵ�����ܹ�˵��ˮ�Ļ�ѧʽΪ��![]() ����ʵ��������______
����ʵ��������______
![]() ˵��ˮ�ǻ������ʵ����ʵ��______
˵��ˮ�ǻ������ʵ����ʵ��______
![]() д��˫��ˮ��ȡ�����Ļ�ѧʽ����ʽ______��ˮ�������⺬����ͬ��Ԫ�أ����ǻ�ѧ���ʲ�ͬ��ԭ����______��
д��˫��ˮ��ȡ�����Ļ�ѧʽ����ʽ______��ˮ�������⺬����ͬ��Ԫ�أ����ǻ�ѧ���ʲ�ͬ��ԭ����______��
![]() �������Լ��
�������Լ��![]() ��ˮ���ǣ����ɹ��������õĵ�ˮ����ȴ����
��ˮ���ǣ����ɹ��������õĵ�ˮ����ȴ����![]() ����ˮ��Դ��ÿ����������κ���������˵��һ����Լ��ˮ��Ϊ______��
����ˮ��Դ��ÿ����������κ���������˵��һ����Լ��ˮ��Ϊ______��
���𰸡�����ɫ�ء���ζ�� ͼ2�õ������ͼ1�õ�����Ȼ�ǻ���� ����ˮ ��ѧ ���� �����ǵ�ľ�� ������������ˮ������������ˮ 4 ��ԭ�ӡ���ԭ�� 2H2O![]() 2H2
2H2![]() +O2
+O2![]() ͼ2��ˮ���Ӳ��䣬ͼ3��ˮ���ӷֽ���������Ӻ������� �����������������Ϊ2��1 ���ˮ�������������� 2H2O2
ͼ2��ˮ���Ӳ��䣬ͼ3��ˮ���ӷֽ���������Ӻ������� �����������������Ϊ2��1 ���ˮ�������������� 2H2O2![]() 2H2O+O2
2H2O+O2![]() ���Ӳ�ͬ ����ϴ��ˮ����
���Ӳ�ͬ ����ϴ��ˮ����
��������
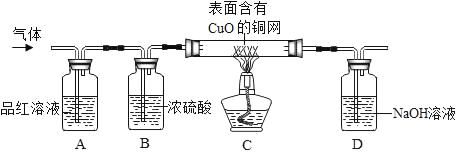
![]() ͼ1Ϊ����ˮװ�ã����л���̿������������ɫ�ء���ζ�ȡ��������ɫ�ء���ζ�ȡ�
ͼ1Ϊ����ˮװ�ã����л���̿������������ɫ�ء���ζ�ȡ��������ɫ�ء���ζ�ȡ�
![]() ��ˮ�ֱ�ͼ2��ͼ1װ�õ�������������ˮ�ʳɷֵ�������ͼ2�õ�������ˮ��ͼ1�õ�����Ȼ�ǻ���������Ϊ�������ܳ�ȥ����ˮ�����ʡ����ͼ2�õ������ͼ1�õ�����Ȼ�ǻ���
��ˮ�ֱ�ͼ2��ͼ1װ�õ�������������ˮ�ʳɷֵ�������ͼ2�õ�������ˮ��ͼ1�õ�����Ȼ�ǻ���������Ϊ�������ܳ�ȥ����ˮ�����ʡ����ͼ2�õ������ͼ1�õ�����Ȼ�ǻ���
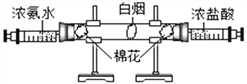
![]() ��ˮ�м������ˮʱ�������������ĭ�϶࣬����ˮ���������������������Ӳˮ����˿����÷���ˮ������ͼ1����õ�ˮ�Ƿ�ΪӲˮ���������ˮ��
��ˮ�м������ˮʱ�������������ĭ�϶࣬����ˮ���������������������Ӳˮ����˿����÷���ˮ������ͼ1����õ�ˮ�Ƿ�ΪӲˮ���������ˮ��
![]() ͼ3Ϊ����ˮ����������ˮ�Ĺ����е���ת��Ϊ��ѧ�ܡ������ѧ��
ͼ3Ϊ����ˮ����������ˮ�Ĺ����е���ת��Ϊ��ѧ�ܡ������ѧ��
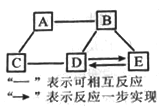
![]() ͨ��һ��ʱ���A�Թ��в��������������������ô����ǵ�ľ������A���е����壬������Ϊ������ʹ�����ǵ�ľ����ȼ����������������ǵ�ľ����
ͨ��һ��ʱ���A�Թ��в��������������������ô����ǵ�ľ������A���е����壬������Ϊ������ʹ�����ǵ�ľ����ȼ����������������ǵ�ľ����
![]() ��B�������ɵ�����ۼ����ϲ���ԭ����������������ˮ������������ˮ��
��B�������ɵ�����ۼ����ϲ���ԭ����������������ˮ������������ˮ��
A�ܺ�B����������֮��Ϊ1��2����A�����ռ�2L�����壬��B�����ռ����������ԼΪ4L�����������������ˮ������������ˮ��4��
![]() ˮ�ķֽ�����У��������ı��������ԭ�ӡ���ԭ�ӡ������ԭ�ӡ���ԭ�ӡ�
ˮ�ķֽ�����У��������ı��������ԭ�ӡ���ԭ�ӡ������ԭ�ӡ���ԭ�ӡ�
![]() ���ˮ������������������Ӧ�Ļ�ѧ����ʽΪ��
���ˮ������������������Ӧ�Ļ�ѧ����ʽΪ��![]() �����
�����![]() ��
��
![]() ���۵ĽǶȽ���ͼ2��ͼ3�еķ����仯�ı��ʲ�ͬ��ͼ2��ˮ���Ӳ��䣬ͼ3��ˮ���ӷֽ���������Ӻ������ӡ�
���۵ĽǶȽ���ͼ2��ͼ3�еķ����仯�ı��ʲ�ͬ��ͼ2��ˮ���Ӳ��䣬ͼ3��ˮ���ӷֽ���������Ӻ������ӡ�
���ͼ2��ˮ���Ӳ��䣬ͼ3��ˮ���ӷֽ���������Ӻ������ӡ�
![]() ��֪ͬ��ͬѹ�£�����������ȡ��������ķ��Ӹ����ȣ���ʵ�����ܹ�˵��ˮ�Ļ�ѧʽΪ��
��֪ͬ��ͬѹ�£�����������ȡ��������ķ��Ӹ����ȣ���ʵ�����ܹ�˵��ˮ�Ļ�ѧʽΪ��![]() ����ʵ�������������������������Ϊ2��1��
����ʵ�������������������������Ϊ2��1��
��������������������Ϊ2��1��
![]() ˵��ˮ�ǻ������ʵ����ʵ�ǵ��ˮ����������������
˵��ˮ�ǻ������ʵ����ʵ�ǵ��ˮ����������������
������ˮ����������������
![]() ���������ڶ������̴������·ֽ�����ˮ����������Ӧ�Ļ�ѧ����ʽΪ��
���������ڶ������̴������·ֽ�����ˮ����������Ӧ�Ļ�ѧ����ʽΪ��![]() ��
��
ˮ�������⺬����ͬ��Ԫ�أ����ǻ�ѧ���ʲ�ͬ��ԭ���Ƿ��Ӳ�ͬ��
���![]() �����Ӳ�ͬ��
�����Ӳ�ͬ��
![]() ��Լ��ˮ��Ϊ������ϴ��ˮ����������ˮ��ʹ�رտ��صȡ��������ϴ��ˮ������
��Լ��ˮ��Ϊ������ϴ��ˮ����������ˮ��ʹ�رտ��صȡ��������ϴ��ˮ������

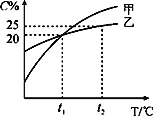
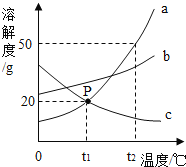
����Ŀ��Fenton�������ڴ������ѽ����л���Ĺ�ҵ��ˮ����ԭ��������Fe2+��H2O2��Ӧ�����ܽ�����Ⱦ��Ļ��Գɷ֡������ø÷��������л���Ⱦ��p-CP��̽���й����ضԽ��ⷴӦ���ʵ�Ӱ�졣ʵ��ʱ��p-CP�ij�ʼŨ����ͬ���¶Ⱥ�Ϊ25���40�森ʵ����p-CP��Ũ����ʱ��仯�Ĺ�ϵ��ͼ��
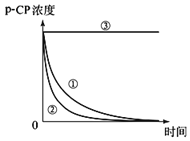
��ش�
��1�����������ʵ����Ʊ���
ʵ�� ��� | ʵ��Ŀ�� | �¶�/�� | pH | Ũ��/��mgL-1�� | |
H2O2 | Fe2+ | ||||
�� | Ϊ�ڢ��ṩ���� | 25 | 3 | 204 | 16.8 |
�� | ̽���¶ȶԽ��ⷴӦ���ʵ�Ӱ�� | ______ | 3 | 204 | 16.8 |
�� | ̽����ҺpH�Խ��ⷴӦ���ʵ�Ӱ�� | 25 | 10 | 204 | 16.8 |
��2��ʵ��١��ڱ����¶����ߣ����ⷴӦ����______��
��3����һ��ʵ�鷢�֣��¶ȹ���ʱ�����ⷴӦ���ѷ�������������Լ�H2O2�ĽǶȷ���ԭ��______��
��4��Ϊ�ⶨ��ͬʱ�����л��オ���Ũ�ȣ����ڲ�ͬʱ��ӷ�Ӧ����ȡ������ʹ��ȡ��Ʒ�еĽ��ⷴӦ����ֹͣ������ͼʾ��Ϣ����д��Ѹ��ֹͣ��Ӧ��һ�ַ�����______��