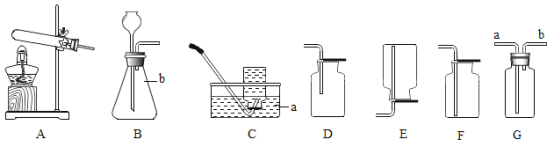
题目内容
【题目】氨(NH3)的催化氧化是工业制取硝酸的重要反应。下图是氨催化氧化的微观模型图。
(1)请把下图中的微观粒子补画完整_______。
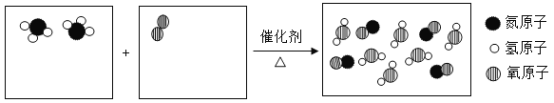
(2)上述模型图说明化学反应前后没有发生变化的粒子是_____________。
(3)写出上述反应的化学方程式___________。
【答案】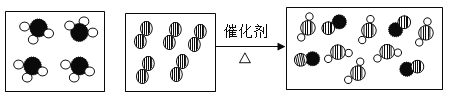 氮原子、氢原子、氧原子 4NH3+5O2
氮原子、氢原子、氧原子 4NH3+5O2 4NO+6H2O
4NO+6H2O
【解析】
(1)由微观粒子反应示意图可知:氨气分子与氧气分子在一定条件下反应产生4个一氧化氮分子和6个水分子;该反应符合质量守恒定律,则化学方程式为:4NH3+5O2 4NO+6H2O;微观粒子补画图:
4NO+6H2O;微观粒子补画图: ;
;
(2)原子是化学变化中的最小粒子,模型图说明化学反应前后没有发生变化的粒子是:氮原子、氢原子、氧原子;
(3)氨气与氧气在催化剂加热的条件下生成一氧化氮和水:4NH3+5O2 4NO+6H2O。
4NO+6H2O。

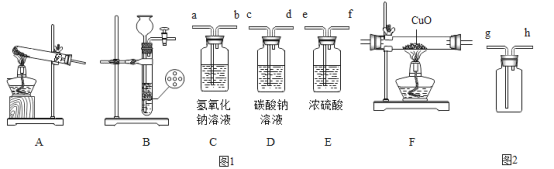
【题目】实验中学兴趣小组关注智利救援33名矿工的时事新闻。兴趣小组设计出空气中氧气含量的测定实验,实验装置如下图所示,请你与兴趣小组共同完成下列科学探究:
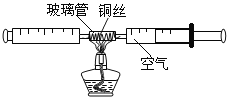
(实验设计)
(1)在由两个注射器组成的密闭系统中留有25mL空气,给装有细铜丝的玻璃管加热,同时缓慢推动两个注射器活塞,至玻璃管内的铜丝在较长时间内无进一步变化时停止加热;
(2)待冷却至室温,将气体全部推至一个注射器内,观察密闭系统内空气体积变化。
(实验操作)
(1)在实验加热过程中,交替缓慢推动两个注射器活塞的目的是_____________。
(2)写出该实验中反应的化学方程式为_____________,反应的基本类型是________。
(数据分析)该兴趣小组测得实验结果如下:
反应前注射器内气体总体积 | 反应后注射器内气体总体积 |
25mL | 22mL |
(1)由此数据可以推算出小组测定的空气中氧气的体积分数____ 2l%(填“>”、“=”、“<”)。
(2)该实验探究只是粗略测定空气中氧气含量的一种方法,你认为实验不够精确,造成该实验出现误差的原因可能是___________。(填序号)
①没有交替缓缓推动两个注射器活塞;②读数时没有冷却至室温;③加入铜丝量太少;④加入铜丝量太多;⑤装置气密性不好
(共同归纳)
通过上面的实验,你学到的测量混合物中某成分含量的方法是____________。
【题目】某造纸厂排放的废水中含有Na2CO3和NaOH。为测定废水中Na2CO3的质量分数,取50g废水样品于烧杯中,将40g稀盐酸分成4等份分4次缓慢加入到烧杯中,产生气体质量与稀盐酸溶液的质量关系如图曲线所示。回答下列问题:
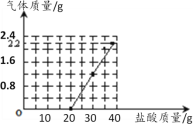
(1)请仔细分析如图数据,完成下表实验记录:
实验次数 | 1 | 2 | 3 | 4 |
稀盐酸的质量(g) | 10 | 10 | 10 | 10 |
生成气体质量(g) | 0 | ____ | ____ | ____ |
(2)上述生成气体________ g。
(3)计算该废水中Na2CO3的质量分数________。
(4)测定Na2CO3的质量分数,也可用下列方法:另取上述废水样品50g,向废水中逐滴加入CaCl2溶液,至反应完全时,经过滤、洗涤、干燥、_________,即可计算出Na2CO3的质量分数。