题目内容
下图是实验室制取和收集气体的装置图.
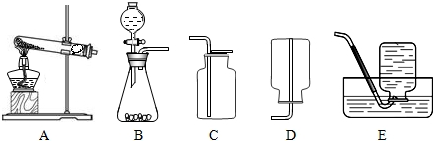
(1)图中有标号的仪器名称:①______;②______.
(2)要在实验室中制取并收集一瓶比较纯净的氧气,可采用______(填序号)组合,其化学反应方程式为______,确定其收集方法的依据是______.
(3)在实验室开放日,某化学兴趣小组5位同学到实验室深入探究二氧化碳的化学性质.
二氧化碳本身不能燃烧,一般也不支持燃烧,常被用做灭火剂.老师指出金属镁着火时不能用二氧化碳灭火,是由于金属镁可在二氧化碳中继续燃烧,生成白色的氧化镁和黑色的碳.小聪同学由此推理:活泼性比镁强的金属钠(Na)也能像镁一样与二氧化碳发生反应,生成的氧化钠和黑色的碳.为了证实小聪同学的推理,兴趣小组的同学在老师的指导下,完成了“钠在二氧化碳中的燃烧”探究实验.
①实验室制取二氧化碳
实验室制取和收集二氧化碳,选择上图装置中的______填序号),其反应的化学方程式为______.若要得到干燥纯净的二氧化碳,可以将发生装置产生的气体先通过装有碳酸氢钠溶液的洗气瓶除去HCl气体,再通过装有浓硫酸的洗气瓶,除去______.
②金属钠在二氧化碳中的燃烧如右图装置所示,图中氯化钯溶液用来检测是否有一氧化碳生成(一氧化碳能与氯化钯(PdCl2)反应生成黑色的钯).切取一薄片金属钠,用滤纸吸干煤油,再除去表面的氧化层放在干燥的硬质玻璃管里.实验开始时先通入干燥的二氧化碳气体,此时PdCl2溶液没明显变化,但澄清石灰水中出现______(填现象),有关反应的化学方程式为______.排尽玻璃管里的空气后,继续通入二氧化碳气体.在玻璃管底部加热,过一会,钠在充满二氧化碳气体的玻璃管里燃烧起来,产生白烟,PdCl2溶液中有黑色物质生成.实验结果表明:金属钠能与二氧化碳发生反应,但生成物中没有黑色的碳,而是一氧化碳.这跟镁与二氧化碳发生反应的结果是不一样的.金属钠与二氧化碳发生反应是否生成氧化钠呢?该兴趣小组同学讨论后认为:金属钠与二氧化碳发生反应生成的白烟可能是氧化钠,也可能是碳酸钠,或者是氧化钠和碳酸钠的混合物.已知氧化钠能与水反应:Na2O+H2O═2NaOH,反应后所得溶液呈现碱性.为了检验金属钠与二氧化碳反应生成的白烟成分,兴趣小组同学进行了如下实验,并根据实验现象得出了结论.
| 实验步骤 | 实验现象 | 结论 |
| 取试管中冷却后的白色固体溶于水,分别置于两支试管中 | 滴加过量______,产生白色沉淀,取上层清液,滴加无色酚酞试液,指示剂没有变色. | 白色固体不可能含有 ______物质 |
滴加______,有气泡产生. | 白色固体是______ |
解:(1)①是支持和固定试管的仪器,是铁架台;②是收集少量气体的仪器,是集气瓶.
(2)实验室制氧气的方法有三种:加热氯酸钾、加热高锰酸钾、过氧化氢分解,前二者是加热固体制气体,发生装置选A,后者是固体与液体常温下混合制气体,发生装置选B,由于要求收集纯净的氧气,收集方法用排水法,装置选E,选择基本依据是氧气不易溶解于水;根据制取原理,相关反应方程式为:2KMnO4 K2MnO4+MnO2+O2↑(或2H2O2
K2MnO4+MnO2+O2↑(或2H2O2 2H2O+O2↑).
2H2O+O2↑).
(3)①实验室制二氧化碳的反应原理是碳酸钙与盐酸反应生成氯化钙、水、二氧化碳,方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;药品是固态的石灰石和液态的稀盐酸,反应不需要加热,发生装置选择B,二氧化碳能溶于水,不能用排水法收集,其密度比空气大,可用向上排空气尖收集,装置选择C;因浓硫酸有吸水性,常作气体干燥剂,用来除去气体中的水蒸气.
②二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,故二氧化碳通入澄清的石灰水,石灰水会变浑,方程式为CO2+Ca(OH)2=CaCO3↓+2H2O;因为Na2O+H2O═2NaOH,在溶液中可通过检验氢氧化钠来检验氧化钠,生成的产物是氧化钠,还是碳酸钠,还是二者的混合物,可以先把固体溶解于水制成溶液,然后加入足量的氯化钙溶液,通过是否有白色沉淀来判断有无碳酸钠,如有碳酸钠并同时除去,最后用指示剂检验是否有氢氧化钠,从而判断是否有氧化钠,当然用盐酸可直接检验是否有碳酸钠;根据实验结果,产物为碳酸钠和一氧化碳,故方程式为2Na+2CO2 Na2CO3+CO.
Na2CO3+CO.
故答案为:(1)①铁架台;②集气瓶;(2)A E (或B E);2KMnO4 K2MnO4+MnO2+O2↑(或2H2O2
K2MnO4+MnO2+O2↑(或2H2O2 2H2O+O2↑); 氧气不易溶于水;
2H2O+O2↑); 氧气不易溶于水;
(3)①BC;CaCO3+2HCl=CaCl2+H2O+CO2↑; 水蒸气;②浑浊;CO2+Ca(OH)2=CaCO3↓+2H2O;
2Na+2CO2 Na2CO3+CO.
Na2CO3+CO.
分析:(1)根据仪器的形状、结构、用途判断.
(2)根据实验室制氧气的原理和方法,以及气体收集装置的选择依据、排水法的优点回答.
(3)①根据实验室制二氧化碳所用药品的状态、反应条件、二氧化碳的性质选择装置;根据反应原理书写方程式;根据浓硫酸的吸水性判断其作用.
②根据二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水的性质回答前两空;根据碳酸钠与可溶性钙盐反应生成碳酸钙白色沉淀,Na2O+H2O═2NaOH,反应后所得溶液呈现碱性回答表格;根据实验结果判断出除一氧化碳外的另一种产物,再写出方程式.
点评:气体的制取是初中重要的化学实验之一,既是难重点,又是考查热点,理解反应原理,掌握装置的选择依据、气体的检验、验满、收集方法,了解实验步骤和注意事项是解决该类问题的关键.
(2)实验室制氧气的方法有三种:加热氯酸钾、加热高锰酸钾、过氧化氢分解,前二者是加热固体制气体,发生装置选A,后者是固体与液体常温下混合制气体,发生装置选B,由于要求收集纯净的氧气,收集方法用排水法,装置选E,选择基本依据是氧气不易溶解于水;根据制取原理,相关反应方程式为:2KMnO4
 K2MnO4+MnO2+O2↑(或2H2O2
K2MnO4+MnO2+O2↑(或2H2O2 2H2O+O2↑).
2H2O+O2↑).(3)①实验室制二氧化碳的反应原理是碳酸钙与盐酸反应生成氯化钙、水、二氧化碳,方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;药品是固态的石灰石和液态的稀盐酸,反应不需要加热,发生装置选择B,二氧化碳能溶于水,不能用排水法收集,其密度比空气大,可用向上排空气尖收集,装置选择C;因浓硫酸有吸水性,常作气体干燥剂,用来除去气体中的水蒸气.
②二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,故二氧化碳通入澄清的石灰水,石灰水会变浑,方程式为CO2+Ca(OH)2=CaCO3↓+2H2O;因为Na2O+H2O═2NaOH,在溶液中可通过检验氢氧化钠来检验氧化钠,生成的产物是氧化钠,还是碳酸钠,还是二者的混合物,可以先把固体溶解于水制成溶液,然后加入足量的氯化钙溶液,通过是否有白色沉淀来判断有无碳酸钠,如有碳酸钠并同时除去,最后用指示剂检验是否有氢氧化钠,从而判断是否有氧化钠,当然用盐酸可直接检验是否有碳酸钠;根据实验结果,产物为碳酸钠和一氧化碳,故方程式为2Na+2CO2
 Na2CO3+CO.
Na2CO3+CO.故答案为:(1)①铁架台;②集气瓶;(2)A E (或B E);2KMnO4
 K2MnO4+MnO2+O2↑(或2H2O2
K2MnO4+MnO2+O2↑(或2H2O2 2H2O+O2↑); 氧气不易溶于水;
2H2O+O2↑); 氧气不易溶于水;(3)①BC;CaCO3+2HCl=CaCl2+H2O+CO2↑; 水蒸气;②浑浊;CO2+Ca(OH)2=CaCO3↓+2H2O;
| 实验步骤 | 实验现象 | 结论 |
| CaCl2 溶液 | Na2O | |
| 稀HCl | Na2CO3 |
 Na2CO3+CO.
Na2CO3+CO.分析:(1)根据仪器的形状、结构、用途判断.
(2)根据实验室制氧气的原理和方法,以及气体收集装置的选择依据、排水法的优点回答.
(3)①根据实验室制二氧化碳所用药品的状态、反应条件、二氧化碳的性质选择装置;根据反应原理书写方程式;根据浓硫酸的吸水性判断其作用.
②根据二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水的性质回答前两空;根据碳酸钠与可溶性钙盐反应生成碳酸钙白色沉淀,Na2O+H2O═2NaOH,反应后所得溶液呈现碱性回答表格;根据实验结果判断出除一氧化碳外的另一种产物,再写出方程式.
点评:气体的制取是初中重要的化学实验之一,既是难重点,又是考查热点,理解反应原理,掌握装置的选择依据、气体的检验、验满、收集方法,了解实验步骤和注意事项是解决该类问题的关键.

练习册系列答案
相关题目




