题目内容
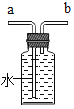
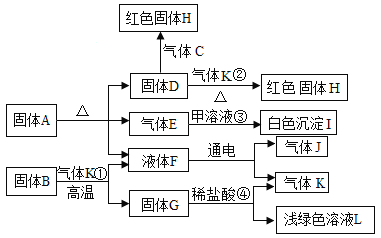
【题目】获悉某处矿井中瓦斯报警器发出警报后,学校兴趣小组请求该矿井安全监测人员提供了少量气体样品,进行成分探究。兴趣小组经资料查询,通常瓦斯气体可能含有CO、CO2、CH4等气体。为确定该气体是否含有这三种气体中的一种或几种,小组组长初步设计了如下实验方案供大家讨论:
(已知:![]() )
)
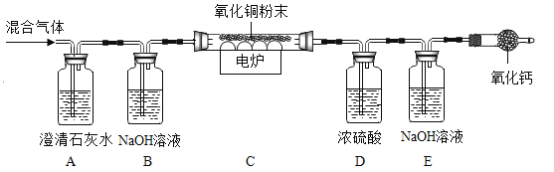
(1)实验装置末端干燥管中氧化钙的作用是______;
(2)同学乙认为,若装置C中CuO变红,则除了甲烷与CuO可能发生反应外,还可能发生的反应是___(用化学方程式表示);
(3)同学丙认为,欲通过D装置中浓硫酸因吸收水分而增重,说明混合气体中含有CH4的思路不严密,认为需要在____(填序号)间再增加一个D装置(编号为F),才能证明含有CH4;
(4)同学丁认为,B装置可有可无。说说你的看法和理由______;
(5)同学戊认为,该装置存在着___重大安全隐患,小组成员一致同意。
综合上述讨论,兴趣小组将经过安全处理后的混合气体,通过改进后的装置进行了实验探究,请根据实验现象和数据填写结论:
装置 | 实验现象/数据 | 实验结论 |
A | 石灰水变浑浊 | 通过实验现象和数据,小组成员一致认为该气体样品中含有______。 |
B | 无明显现象 | |
C | 黑色粉末变成红色 | |
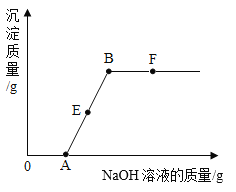
D | 装置D增重3.6g | |
E | 装置E增重4.4g |
【答案】防止空气中的水蒸汽和二氧化碳进入E装置(答案合理即可) ![]() BC 装置B必须有,因为Ca(OH)2微溶,装置A不能保证CO2吸收完全 可燃性气体中含有氧气,加热时可能爆炸 CO2、CH4
BC 装置B必须有,因为Ca(OH)2微溶,装置A不能保证CO2吸收完全 可燃性气体中含有氧气,加热时可能爆炸 CO2、CH4
【解析】
根据一氧化碳具有还原性、气体通过石灰水和氢氧化钠溶液时会带出水蒸气、碱的化学性质和化学方程式计算物质的质量比,进行分析作答。
(1)实验装置末端干燥管中氧化钙的作用是防止空气中的水蒸汽和二氧化碳进入E装置;
(2)一氧化碳具有还原性,能与氧化铜反应,还可能发生的反应是![]() ;
;
(3)气体通过A石灰水和B氢氧化钠溶液时会带出水蒸气,需要在BC间再增加一个D装置,来吸收水蒸气;
(4)装置B必须有,因为Ca(OH)2微溶于水,装置A不能保证CO2吸收完全,需用氢氧化钠溶液来完全吸收二氧化碳;
(5)同学戊认为,该装置存在着:可燃性气体中含有氧气,加热时可能发生爆炸的重大安全隐患;
根据实验现象A中石灰水变浑浊,说明原气体中含有二氧化碳;黑色粉末变成红色,说明含有还原性的气体;装置D增重3.6g,装置E增重4.4g,说明一定有甲烷;通过数据分析判断是否含有一氧化碳;甲烷和氧化铜的反应为: ![]() ,通过方程式得到产生二氧化碳和水的质量比是:44:(2×18)=44:36,装置E增重4.4g,装置D增重3.6g,即生成了4.4g二氧化碳和3.6g水,质量比为4.4g:3.6g=44:36,所以只含有甲烷,不含一氧化碳;通过实验现象和数据,小组成员一致认为该气体样品中含有CO2、CH4。
,通过方程式得到产生二氧化碳和水的质量比是:44:(2×18)=44:36,装置E增重4.4g,装置D增重3.6g,即生成了4.4g二氧化碳和3.6g水,质量比为4.4g:3.6g=44:36,所以只含有甲烷,不含一氧化碳;通过实验现象和数据,小组成员一致认为该气体样品中含有CO2、CH4。

 阅读快车系列答案
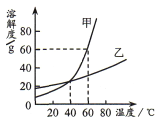
阅读快车系列答案【题目】KCl和KNO3在不同温度下的溶解度数据如表所示,下列说法中正确的是
温度/℃ | 20 | 30 | 60 | |
溶解度/g | KCl | 33 | 38 | 45 |
KNO3 | 31 | 64 | 110 |
A. 60℃时,100g水中最多溶解45 g KCl
B. 随着温度的升高,某饱和KCl溶液中会有固体析出
C. KNO3的溶解度始终大于KCl
D. 60℃时,某KNO3溶液中溶质的质量分数一定为 ![]()