题目内容
【题目】甲、乙、丙为初中常见物质,其转化关系如下图(“→”表示由一种物质转化成另一种物质,反应条件、部分反应物和生成物已略去)。
![]()
(1)若甲,乙、丙均含有同一种金属元素,人体缺少它会贫血,甲为单质,乙含有两种元素,丙含有三种元素,则丙可能是_____。
(2)若甲、乙、丙均为含有钙元素的化合物,甲与水反应生成乙并放出大量的热。甲的俗称是_____。则甲→乙的化学方程式为_____,丙可能是_____(写一种)。
(3)若甲、乙、丙为氧化物,除氧元素外另一种元素均不相同,且三种物质常温下依次为固态、气态和液态,则甲可能是_____(写一种)。
【答案】Fe2(SO4)3 生石灰 CaO+H2O=Ca(OH)2 CaCl2/CaCO3/CaSO4 Fe2O3/CuO
【解析】
(1)若甲,乙、丙均含有同一种金属元素,人体缺少铁会贫血,甲为单质是铁,乙丙是含铁元素的化合物。
(2)若甲、乙、丙均为含有钙元素的化合物,氧化钙与水反应生成乙,并放出大量的热。
(3)常温下,常见液体氧化物是水,气体氧化物可能是二氧化碳,固体氧化物可能是氧化铁或者氧化铜。
(1)甲为单质是铁,铁生锈生成氧化铁,氧化铁和硫酸反应生成硫酸铁,丙含有三种元素,则丙可能是硫酸铁。
(2)甲是氧化钙,俗称是生石灰;氧化钙和水反应生成氢氧化钙,化学方程式为CaO+H2O=Ca(OH)2;氢氧化钙和二氧化碳反应生成碳酸钙,丙可能是碳酸钙。
(3)常温下液体氧化物可能是水,气体氧化物可能是二氧化碳、一氧化碳等,固体氧化物可能是氧化铁或者氧化铜。氧化铜和一氧化碳反应生成二氧化碳,二氧化碳和氢氧化钠溶液反应生成碳酸钠和水。故甲可能是氧化铜。

【题目】(7分)某同学在实验室发现了一瓶标签残缺的无色溶液﹙如图甲所示﹚,为确认其中的溶质,他设计并进行了如下探究活动,请回答下列问题。
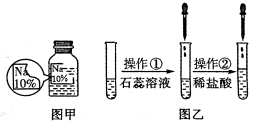
【猜想与假设】其溶质可能为NaCl、NaOH、Na2CO3和NaHCO3中的一种。
【资料查阅】上述四种物质的相关信息如下:
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
常温下某稀溶液的pH | 7 | 13 | 11 | 9 |
【探究过程】
如图乙所示,在操作①后可确定溶质不是NaCl,则其实验现象应是 ;
在进行操作②时有无色无味得到气体产生,由此又可排除假设物质中的 。
【探究结论】
你认为该溶液中的溶质可能是上述假设物质中的 ,你的判断依据是 。
【探究反思】
(1)若上述探究结论是正确的,操作②产生的气体应是 (写化学式),实验室检验该气体的实验操作及现象是 。
(2)另有同学猜想其中的溶质还可能是Na2SO4,但又没有Na2SO4的上述表列信息。
请你根据以上实验操作的相关现象,判断该溶液中的溶质是否是Na2SO4,并叙述理由: 。