��Ŀ����
����Ŀ����Դ��������������ͷ�չ���ɻ�ȱ�����ء�
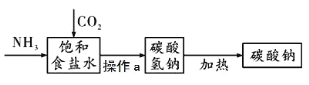
��1��Ϊ��������β���Կ�������Ⱦ����Ȼ���ѳ��Դ���������Ϊ������ȼ�ϡ���Ȼ����Ҫ�ɷ��Ǽ��飬д������ȼ�յĻ�ѧ����ʽ_____��
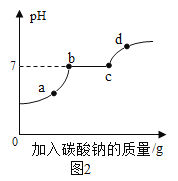
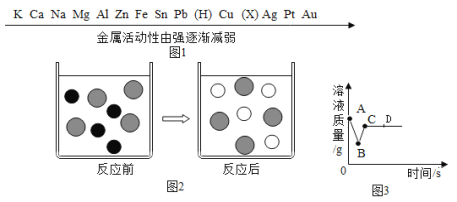
��2�����б仯�����У�������ѧ�仯�����¶����ߵ���_____������ĸ����
Aľ̿ȼ�� Bϡ��Ũ���� C�����Ʒ���ˮ�� Dþ������ϡ���� Eľ̿�������̼��Ӧ F����粒������ˮ��
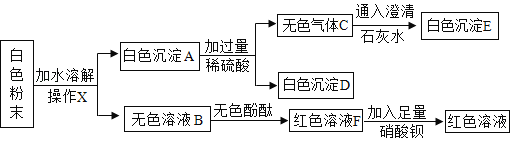
��3��һ�������£���һ���ܱ������ڷ���ij��Ӧ����÷�Ӧǰ������ʵ�������ͼ��ʾ��
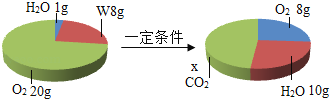
����˵����ȷ����_____������ĸ����
A X��ֵΪ11
B �÷�Ӧ�����û���Ӧ
C ����W������Ԫ�����
D W��̼����Ԫ��ԭ�Ӹ�����Ϊ1��4
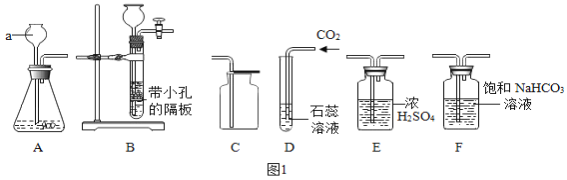
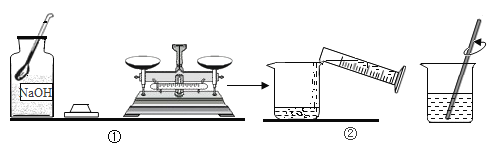
��4��Ǧ������ŵ��ȶ�����۽ϵ͵��ŵ��Ӧ�ù㷺��������Ҫ�õ�������������Ϊ28%��������Һ��ʵ������98%��Ũ���ᣨ�ܶ�1.84g/mL������28%��������Һ1000g����Ҫ98%Ũ��������Ϊ___mL��������������0.1����
���𰸡�CH4+2O2![]() CO2+2H2O ACD ACD 155.3
CO2+2H2O ACD ACD 155.3
��������
��1����Ȼ����Ҫ�ɷ��Ǽ��飬����ȼ�������˶�����̼��ˮ����Ӧ�Ļ�ѧ����ʽ��CH4+2O2![]() CO2+2H2O��
CO2+2H2O��
��2��ľ̿ȼ�ա������Ʒ���ˮ�С�þ������ϡ���ᣬ���ϱ仯�������˻�ѧ�仯�����¶����ߣ�ϡ��Ũ������Һ�¶�����û�з�����ѧ�仯��ľ̿�������̼��Ӧ�������ȷ�Ӧ������粒������ˮ�У���Һ�¶Ƚ��͡�
��3����������������W������������С�������Ƿ�Ӧ��ҷ�Ӧ�����������8g+��20g��8g����20g����ˮ���������ӣ�������ֵ��10g��1g��9g�����������غ㶨�ɲμӻ�ѧ��Ӧ�ĸ����������ܺ͵��ڷ�Ӧ�����ɵĸ����������ܺͣ����Զ�����̼���������������ɵ�������20g��9g��11g���˷�Ӧ�ı���ʽ�ɱ�ʾΪW+O2��CO2+H2O��
A�������Ϸ�����֪��X��ֵΪ11����ȷ��
B���÷�Ӧ�������������ֻ���������û���Ӧ������ȷ��
C�����������غ㶨�ɣ��ɷ�Ӧ����ʽ���Կ���W��һ������̼������Ԫ�أ��Ƿ�����Ԫ����Ҫͨ���������е���Ԫ���뷴Ӧ�������������бȽϣ����ɵ�ˮ����Ԫ�ص�����Ϊ��9g��![]() ��8g��������̼����Ԫ�ص�������11g��
��8g��������̼����Ԫ�ص�������11g��![]() ��8g�����ߵ�������Ϊ16g�����μӷ�Ӧ������������20g��8g��12g�����Կ��ж�W�к�����Ԫ�أ�����W������Ԫ����ɣ���C��ȷ
��8g�����ߵ�������Ϊ16g�����μӷ�Ӧ������������20g��8g��12g�����Կ��ж�W�к�����Ԫ�أ�����W������Ԫ����ɣ���C��ȷ
D��W��̼����Ԫ��ԭ�Ӹ�����Ϊ��![]() ��1��4����ȷ��
��1��4����ȷ��
��4������Ҫ98%Ũ��������Ϊx
28%��1000g��x��98%��1.84g/mL����ã�x��155.3mL

 һ���㶨ϵ�д�
һ���㶨ϵ�д� ��У��ҵ��ϵ�д�
��У��ҵ��ϵ�д� ���ɶ���ܲ��¿�ֱͨ��Уϵ�д�
���ɶ���ܲ��¿�ֱͨ��Уϵ�д�