题目内容
【题目】完成细铁丝在氧气中燃烧的探究活动报告。
操作步骤:
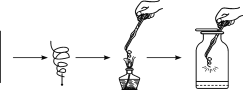
①先用砂纸将铁丝磨成光亮的银白色;
②绕成螺旋状于一根火柴杆上;
③点燃火柴杆、待火柴快燃尽时将铁丝伸入盛有氧气的集气瓶中。
(1)反应的现象是__________
(2)该反应的化学方程式为__________
(3)问题
用收集到的氧气做细铁丝燃烧的实验时,发现瓶底炸裂,发生失误的操作原因可能是__________
【答案】铁丝在氧气中剧烈燃烧,火星四射,放出热量,生成黑色固体 3Fe +2O2![]() Fe3O4 集气瓶底部没有放水或细沙
Fe3O4 集气瓶底部没有放水或细沙
【解析】
(1)铁在氧气中燃烧的实验现象为:剧烈燃烧,火星四射,放出热量,生成黑色固体;故填:铁丝在氧气中剧烈燃烧,火星四射,放出热量,生成黑色固体。
(2)铁和氧气在点燃的条件下生成四氧化三铁,该反应的化学方程式为:3Fe +2O2![]() Fe3O4。故填:3Fe +2O2
Fe3O4。故填:3Fe +2O2![]() Fe3O4。
Fe3O4。
(3)用收集到的氧气做细铁丝燃烧的实验时,应在集气瓶底放少量的水或细沙,防止高温溅落物使瓶底受热不均而炸裂,因此发现瓶底炸裂,发生失误的操作原因可能是集气瓶底部没有放水或细沙;故填:集气瓶底部没有放水或细沙。

【题目】某碳酸钠样品中含有一定量的碳酸氢钠。为测定其纯度,取100 g样品加热至不再产生气体(2NaHCO3![]() Na2CO3 + H2O +CO2↑),使生成的水完全被浓硫酸吸收,测得加热时间和浓硫酸质量增加的关系如下表:
Na2CO3 + H2O +CO2↑),使生成的水完全被浓硫酸吸收,测得加热时间和浓硫酸质量增加的关系如下表:
时间 物质的质量 | 0分钟 | 1分钟 | 2分钟 | 3分钟 | 4分钟 |
仪器和碱石灰的质量总和(g) | 150 | 150.9 | 151.8 | 152.7 | 152.7 |
(1)当完全反应后,生成水的质量为______g
(2)计算样品中碳酸氢钠的质量分数是多少____?
(3)将其完全分解后的物质溶解于300 g水中完全溶解后,计算所得溶液中溶质的质量分数____?