题目内容
【题目】用化学符号表示:
(1)氧化镁中镁为+2价________;
(2)最轻的气体________;
(3)2个氧分子_______________;
(4)2个硫酸根离子________;
(5)-2价的硫元素______________;
(6)2个亚铁离子________。
【答案】![]() H2 2O2 2SO42-
H2 2O2 2SO42- ![]() 2Fe2+
2Fe2+
【解析】
(1)元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,所以氧化镁中镁为+2价,故可表示为:![]() ;
;
(2)最轻的气体是氢气,其化学式为:H2;
(3)2个氧分子就是在氧气化学式的前面加上数字2,故可表示为:2O2;
(4)离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略;若表示多个该离子,就在其元素符号前加上相应的数字,故2个硫酸根离子可表示为:2SO42-;
(5)-2价的硫元素就是在硫元素符号的正上方加上-2,故可表示为:![]() ;
;
(6)离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略,若表示多个该离子,就在其元素符号前加上相应的数字,故2个亚铁离子可表示为:2Fe2+。

【题目】某同学对下表中的溶解度数据分析后,得出的结论正确的是( )
温度/℃ | 0 | 20 | 40 | 60 |
KCl的溶解度/g | 27.6 | 34.0 | 40.0 | 45.5 |
KNO3的溶解度/g | 13.3 | 31.6 | 63.9 | 110 |
Ca(OH)2的溶解度/g | 0.18 | 0.16 | 0.14 | 0.11 |
A.硝酸钾的溶解度最大
B.降温可将不饱和的Ca(OH)2溶液变为饱和溶液
C.40℃时,饱和的氯化钾溶液溶质质量分数为40%
D.当KNO3中混有少量KCl时,可以用冷却热饱和溶液的方法提纯
【题目】铜镁合金具有优良的导电性,常用作飞机天线等导电材料.欲测定合金的组成(其他元素忽略不计),进行如下实验:取铜合金20g放入烧杯,将280g稀硫酸分4次加入烧杯中,充分反应后,测得剩余固体的质量记录如下.请计算:
次数 | 1 | 2 | 3 | 4 |
加入稀硫酸质量/g | 70 | 70 | 70 | 70 |
剩余固体质量/g | 18.2 | 16.4 | 14.6 | 13.2 |
(1)合金中铜、镁的质量比.
(2)所加稀硫酸的溶质的质量分数.(写出计算过程)
【题目】完成下列探究实验.
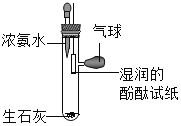
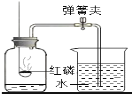
(1)小然同学设计探究分子运动的实验如图1,请按要求完成下列各小题:
①滴入适量浓氨水后,观察到酚酞试纸__________,原因是____.
②放入少量生石灰的作用是____,试写出发生的化学反应方程式____.
(2)有一袋白色粉末,甲同学认为是碳酸钙;乙同学认为是碳酸钠;丙同学认为是碳酸氢钠;丁同学认为是碳酸钠和碳酸氢钠的混合物.为了探究该白色粉末的成分,进行了以下实验:
①将少量白色粉末放入水中搅拌,观察到____,说明甲同学的猜想不正确.
②室温时,分别向盛有等质量的碳酸氢钠、碳酸钠和白色粉末样品的锥形瓶中注入等体积、足量的10%的盐酸,记录如下表:
实验编号 | 锥形瓶内物质 | 最终得到CO2体积/mL | |
名称 | 质量/g | ||
Ⅰ | 碳酸氢钠 | 0.10 | V1 |
Ⅱ | 碳酸钠 | 0.10 | V2 |
Ⅲ | 白色粉末 | 0.10 | V3 |
(解释与结论)
③实验I的化学方程式为_____;
④表中V1___V2(填“>”、“<”或“=”);
⑤若V1>V3>V2则白色粉末物质为_____