题目内容
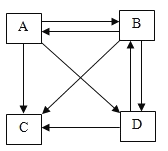
【题目】如下图是某同学画出的四种物质之间的转化关系图。A. B. C. D代表最常见的含有钠离子的四种物质的溶液,“→ ”表示物质间的转化关系,所有的转化关系都可以通过复分解反应实现。请回答下列问题:
(1)钠离子的离子符号是____________;C 中溶质的化学式是_____________。
(2)写出A→B的化学方程式_____________。写出D→C的化学方程式_____________。
【答案】Na+ NaCl (或NaNO3) ![]()
![]() (或
(或![]() )
)
【解析】
根据题目信息,A. B. C. D代表最常见的含有钠离子的四种物质的溶液,结合框图,可推测A是碳酸钠,B是氢氧化钠,C是氯化钠或硝酸钠,D是硫酸钠,代入检验,符合题意。
(1)钠离子的离子符号是Na+;C 中溶质的化学式是NaCl (或NaNO3)。故填:Na+;NaCl (或NaNO3)。
(2)根据以上分析,A. B. C. D代表最常见的含有钠离子的四种物质的溶液,结合框图,可推测A是碳酸钠,B是氢氧化钠,要实现A→B,碳酸钠与氢氧化钙反应可以生成碳酸钙沉淀和氢氧化钠,反应的方程式为![]() ; 因为C是氯化钠或硝酸钠,D是硫酸钠,D→C的反应,硫酸钠可以与氯化钡反应生成硫酸钡和氯化钠,化学方程式为
; 因为C是氯化钠或硝酸钠,D是硫酸钠,D→C的反应,硫酸钠可以与氯化钡反应生成硫酸钡和氯化钠,化学方程式为![]() ,或者硫酸钠与硝酸钡反应生成硝酸钠与硫酸钡,方程式为
,或者硫酸钠与硝酸钡反应生成硝酸钠与硫酸钡,方程式为![]() 。故填:
。故填:![]() (或
(或![]() )。
)。

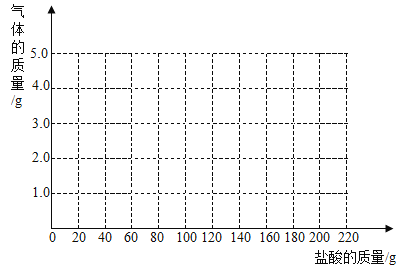
【题目】NaHCO3是初中化学教材中重点介绍的一种盐,俗名称_____,NaHCO3溶液呈碱性。某化学兴趣小组要制取一瓶NaHCO3溶液,他们向NaOH溶液中通了一定量的CO2,然后对反应后所得到的溶液进行探究。
(提出问题)反应后溶液中溶质的成分是什么?
(查阅资料)(1)NaHCO3不仅可以与盐酸反应,也可以与NaOH溶液反应。与NaOH溶液反应的化学方程式为:NaHCO3+NaOH=Na2CO3+H2O。
(2)向NaOH溶液中通入少量CO2,反应的化学方程式为:2NaOH+CO2=Na2CO3+H2O。继续通入过量CO2,反应的化学方程式为:Na2CO3+H2O+CO2=2NaHCO3。
(猜想与假设)猜想一:含有NaOH和Na2CO3;
猜想二:只含有_____;
猜想三:含有Na2CO3和NaHCO3;
猜想四:只含有NaHCO3。
(设计实验)
实验步骤 | 实验现象 | 解释或结论 |
①取少量样品于试管中,滴加几滴无色酚酞溶液 | 溶液呈红色 | 证明溶液显碱性 |
②另取少量样品于试管中,加入足量的BaCl2溶液,反应完全后,静置过滤 | 加入BaCl2溶液时观察到的现象是_____; | 证明溶液中有Na2CO3 |
③向实验②所得的滤液中滴加稀盐酸 | 有无色无味能使澄清石灰水变浑浊的气体产生 | 证明实验②溶液所得的滤液中有_____。 |
(结论与反思)(1)有同学认为实验①观察到的现象及结论足以证明溶液中有NaOH。你是否同意?请先回答再说出理由_____。
(2)写出实验③中产生气体的化学方程式_____。
(3)通过实验①②③所观察到的现象及结论,最终得出猜想_____是正确的。