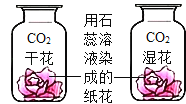
题目内容
【题目】联合国认为提升化学的全球认知至关重要,并将距离门捷列夫发现元素周期律150周年的2019年定为“国际化学元素周期表年”。
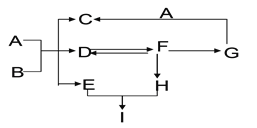
(1)我国科学家张青莲教授主持测定的钢等多种元素的相对原子质量已成为国际标准。根据下图完成下列内容。
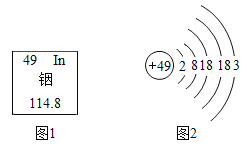
①铟属于_______(填“金属”或“非金属”)元素,其相对原子质量为___________;
②铟的化学性质与铝的化学性质相似,原因是____________;铟元素在元素周期表中位于第__________周期。
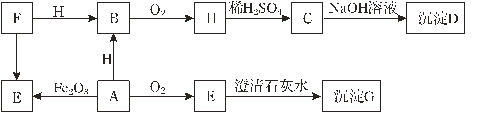
(2)铟与氯气反应生成氯化铟的微观过程如下:
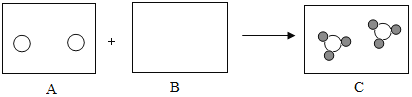
①请将B框中的信息补充完整____________,你这样补充的理由是_________;
②该反应的基本反应类型为_______________。
【答案】金属 114.8 最外层电子数相同 五或5 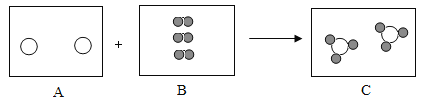 化学反应前后原子的种类、个数不变,一个氯分子由两个氯原子构成;(质量守恒定律) 化合反应
化学反应前后原子的种类、个数不变,一个氯分子由两个氯原子构成;(质量守恒定律) 化合反应
【解析】
(1)①铟元素含有“钅”字旁,属于金属元素,其相对原子质量为114.8;
②铟的化学性质与铝的化学性质相似,原因是最外层电子数相同,都为3个电子;铟元素的原子结构中含有5层电子,电子数=周期数,则在元素周期表中位于第五周期。
(2)铟与氯气反应生成氯化铟的微观过程符合质量守恒定律:
①2个铟原子与3个氯气分子反应产生2个氯化铟;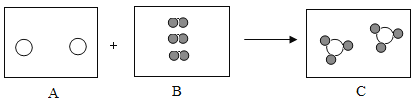 ,补充的理由是化学反应前后原子的种类、个数不变,一个氯分子由两个氯原子构成;
,补充的理由是化学反应前后原子的种类、个数不变,一个氯分子由两个氯原子构成;
②该反应符合“多变一”,属于化合反应。

【题目】红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示。同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究。

(提出问题)久置固体的成分是什么?
(查阅资料)铁与氯化铁溶液在常温下发生反应生成氯化亚铁。
(猜想)久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3。
(实验探究1)甲同学的方案:
实验操作 | 实验现象 | 实验结论 |
(1)取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液 | 固体溶解时试管外壁发烫,试管底部有不溶物,溶液变红 | 固体中一定含有____和Ca(OH)2. |
(2)另取少量固体放于试管中,滴加足量的____ | 固体逐渐消失,有无色气体产生,得到浅绿色溶液 | 固体中一定含有Fe,一定不含Fe2O3 |
(3)将步骤(2)中产生的气体通入到澄清石灰水中 | ____ | 固体中一定含有CaCO3 |
(实验质疑)
(1)乙同学认为甲同学的实验中不能得出一定含Ca(OH)2的结论,理由是_____。
(2)丙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是_____。
(实验探究2)
乙、丙同学设计如下实验方案继续验证:
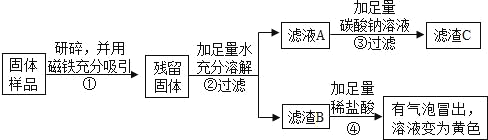
(1)③中反应的化学方程式是_____。
(2)乙、丙同学实验中能得出固体样品中一定还含有_____,仍有一种物质不能确定,该物质是_____。
(3)乙、丙同学又经过实验测得上述残留固体中含钙物质的总质量为1.6g,滤渣B中CaCO3的质量为1.0g,滤渣C的质量为1.0g。
(实验结论)综合上述实验及所给数据,久置固体的成分是_____。
【题目】KCl和KNO3在不同温度下的溶解度数据如表所示,下列说法中正确的是( )
温度/℃ | 20 | 30 | 40 | |
溶解度/g | KCl | 33 | 38 | 45 |
KNO3 | 31 | 64 | 110 |
A.40℃时,100g水中最多溶解45gKCl
B.随着温度的升高,某饱和KCl溶液中会有固体析出
C.KNO3的溶解度始终大于KCl
D.40℃时,某KNO3溶液中溶质的质量分数一定为 ![]() ×100%
×100%