题目内容
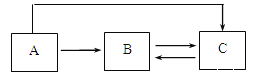
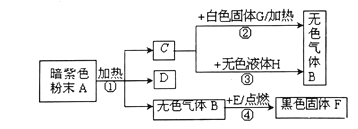
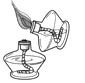
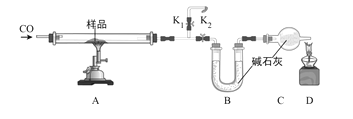
【题目】下图是一些常见物质间互相转化的关系图(图中有些反应条件未注明),A是一种暗紫色固体,反应③自然界最重要的化学变化。查阅资料:含钾元素的化合物均可溶于水。
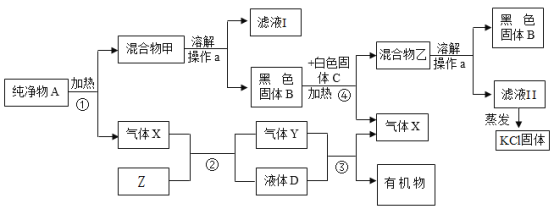
(1)操作a名称是_____,此操作中玻璃棒的作用是_____。
(2)混合物甲和混合物乙中都含的物质是_____(写化学式),写出它与白色固体C混合加热的化学方程式_____。
(3)Z中一定含有的元素是_____(写元素符号),且Z_____(选填字母编号)
a.只能是纯净物 b.只能是混合物 c.既可能是纯净物,也可能是混合物
(4)将气体Y通入液体D中也能发生反应,生成的产物是_____(写化学式)。与反应③比较,反应物相同,_____不同,生成物不同。
【答案】过滤 引流 MnO2 2KClO3![]() 2KCl + 3O2 ↑ C、H c H2CO3 反应条件
2KCl + 3O2 ↑ C、H c H2CO3 反应条件
【解析】
反应③自然界最重要的化学变化,反应③是光合作用,气体Y和液体D反应会生成气体X和葡萄糖,二氧化碳和水在光合作用的条件下生成葡萄糖和氧气,所以Y是二氧化碳,D是水,X是氧气;纯净物A加热会生成氧气和混合物,所以A是高锰酸钾(如果A是氯酸钾,生成物甲是氯化钾,不是混合物),高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,甲就是锰酸钾和二氧化锰的混合物,经过溶解及操作a后,得到滤液]和黑色固体B,判断出操作a是过滤;锰酸钾可溶,所以B是二氧化锰;二氧化锰和氯酸钾在加热的条件下生成氯化钾和氧气,所以混合物乙中含有氯化钾和二氧化锰。将推理结果代入流程图,推理成立。
(1)根据以上分析可知:操作a名称是过滤,此操作中玻璃棒的作用是引流;
(2)混合物甲和混合物乙中都含的物质是二氧化锰,化学式为MnO2,它与白色固体C混合加热反应是二氧化锰和氯酸钾在加热的条件下生成氯化钾和氧气,反应的化学方程式为:2KClO3![]() 2KCl + 3O2 ↑;
2KCl + 3O2 ↑;
(3)X(氧气)与Z反应生成水和二氧化碳,根据质量守恒定律可知,Z中一定含有的元素是C、H,Z既可能是纯净物,也可能是混合物。故选c;
(4)将气体Y(二氧化碳)通入液体D(水)中也能发生反应,生成的产物是碳酸,化学式为H2CO3;与反应③比较,反应物相同,反应条件不同,生成物不同。

 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案【题目】实验设计是化学实验的重要环节.请根据下列实验要求回答相关问题:
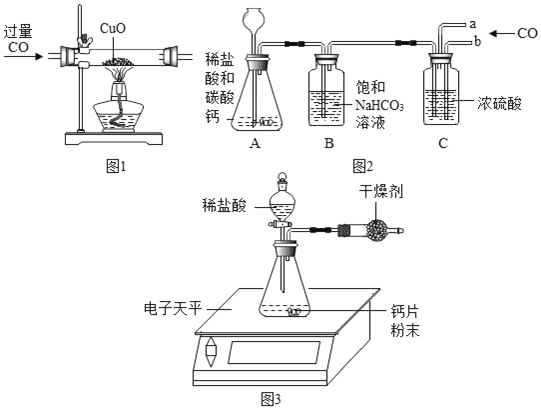
(活动与探究一)收集不同体积比例的二氧化碳和一氧化碳混合气体.
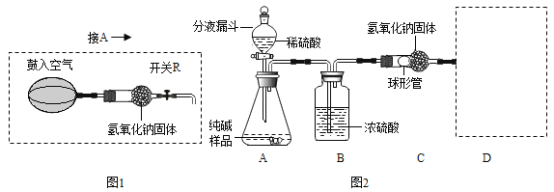
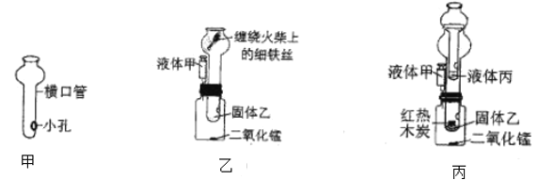
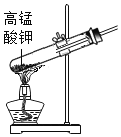
方案一:如图1所示
(1)请写出硬质玻璃管中发生反应的化学方程式_____;
(2)该实验能获得二氧化碳和一氧化碳混合气体,其原因是_____;
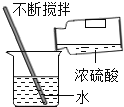
方案二:根据如图2装置所示请回答下列问题:(提示:饱和NaHCO3溶液的作用是除去HCl气体,部分夹持装置及导管已略去)
(1)写出装置A中发生反应的化学方程式:_____.
(2)CO气体应由_____(填“a”或“b”)通入,在C中混合后,由另一导管导出.
(3)装置C中浓硫酸的两点主要作用:
①干燥气体,减少实验误差;②_____.
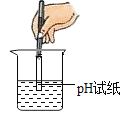
测定某钙片(主要成分CaCO3)中碳酸钙的质量分数,用如图3装置进行如下实验:①取研碎后的钙片4克,倒入气密性良好的锥形瓶中,然后在分液漏斗中加入过量的稀盐酸,置于电子天平上测出装置总质量.②打开活塞,滴入足量稀盐酸后关闭活塞,待气泡不再冒出时,测出反应后装置总质量.③整理相关数据如下表
反应前总质量(克) | 275.58 |
反应后总质量(克) | 274.92 |
(1)小明结合表中数据,计算该钙片中碳酸钙的质量分数.(其它成分不与盐酸反应).
(2)该实验中,如果装置中不加固态干燥剂(干燥剂的作用:吸水但不吸二氧化碳),则最终所算得钙片中碳酸钙的质量将_____(填“偏大”“偏小”或“不变”).